题目内容
17. 草酸钙(化学式为CaC2O4,相对分子质量为128)是一种难溶于水的白色固体,受热能分解.小红同学为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量随时间变化如图所示.请回答下列问题:
草酸钙(化学式为CaC2O4,相对分子质量为128)是一种难溶于水的白色固体,受热能分解.小红同学为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量随时间变化如图所示.请回答下列问题:(1)t1~t2时问段内固体质量减少的原因是产生了一种极易与血红蛋白结合的有毒气体,该气体的化学式为CO;同时生成一种白色同体,它与大理石的主要成分相同,则该段时问内反应的化学方程式为CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑.
(2)t2~t3时间段内固体质量不变的原因是草酸钙已完全分解,但尚未达到碳酸钙的分解温度.
(3)t3~t4时间段内反应的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(4)小强和小明另取12.8g草酸钙固体加热一段时间后,对剩余固体的成分进行探究.
【查阅资料】CaC2O4能与稀盐酸反应,其反应的化学方程式为:CaC2O4+2HCl=CaCl2+H2C2O4;草酸(H2C2O4)是一种可溶于水的酸.
【设计方案并实验】
| 同学 | 实验操作 | 实验现象 | 结论 |
| 小强 | 取少量固体放入烧杯中,加适量水并搅拌 | 烧杯发热 | 剩余固体中一定含有CaO(或氧化钙). 一定不含有CaC2O4. |
| 小明 | 另取少量固体放入试管中,加足量稀盐酸 | 有气体产生 | 剩余固体中一定含有CaCO3(或碳酸钙). |
分析 (1)在t1~t2时间段内,加热草酸钙时产生了极易与血红蛋白结合的有毒气体,此气体是一氧化碳,一种白色固体与大理石的主要成分相同,应是碳酸钙,因此,在加热草酸钙时,草酸钙易分解为碳酸钙和一氧化碳;
(2)当草酸钙完全分解而又未达到碳酸钙分解的温度时,剩余固体的质量不变,这就是在t2~t3时间段内剩余固体质量不变的原因;
(3)当对上述固体继续加热时,生成的碳酸钙又分解为氧化钙和二氧化碳,由于放出二氧化碳又会使剩余固体的质量减少;
(4)向清液中加入紫色石蕊试液,试液变成蓝色,溶液显碱性,溶液显碱性的原因是由于剩余固体中生成的氧化钙和水反应生成氢氧化钙,因为溶液显碱性,一定没有草酸钙;向剩余固体中加入稀盐酸,有气体产生,可推出剩余固体中一定有碳酸钙.综上所述,剩余固体中有氧化钙、碳酸钙.由于碳酸钙未完全分解,小强和小明加热的草酸钙的剩余物与t3~t4时间段的物质成分相同.
解答 解:(1)在 t1~t2时问段内:产生了一种极易与血红蛋白结合的有毒气体,该气体是一氧化碳,化学式是CO;产生的一种白色固体,它与大理石的主要成分相同,这种那白色固体是碳酸钙.发生反应的方程式是:CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑
(2)碳酸钙分解的温度要高于草酸钙分解的温度,当草酸钙完全分解,而温度又未达到碳酸钙的分解温度时,固体的质量不变,所以,t2~t3时间段内固体质量不变.
(3)在t3~t4时间段内,碳酸钙发生了分解,方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
(4)向清液中加入紫色石蕊试液,试液变成蓝色,溶液显碱性,溶液显碱性的原因是由于剩余固体中的氧化钙和水反应生成氢氧化钙,因为溶液显碱性,一定没有草酸钙;通过向剩余固体中加入稀盐酸,有气体产生,可推出剩余固体中一定有碳酸钙.综上所述,剩余固体中由氧化钙、碳酸钙,与t3~t4时间段的物质成分相同.
故答为:(1)CO,CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑
(2)草酸钙已完全分解,但尚未达到碳酸钙的分解温度
(3)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
(4)
| 同学 | 实验操作 | 实验现象 | 结论 |
| 小强 | CaO(或氧化钙) | ||
| 小明 | CaCO3(或碳酸钙) |
点评 本题通过实验探究了草酸钙的性质和变化规律.草酸钙受热易分解生成了碳酸钙和一氧化碳,因为放出了一氧化碳,剩余固体的质量减少.当草酸钙完全分解后继续加热一段时间后,剩余固体的质量又减少,这时一定要联想我们已学过的知识碳酸钙高温也能分解为氧化钙和放出二氧化碳,也会造成剩余固体质量的减少,这是解答本题的关键.

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案| A. | 只含碳一种元素 | B. | 只含氢一种元素 | ||
| C. | 一定含碳和氢两种元素 | D. | 可能含碳、氢、氧三种元素 |
| A. | ①②④ | B. | ①③⑤ | C. | ①③⑥ | D. | ②③⑥ |
【猜想】
A.CuO不是催化剂,也不参加反应,反应前后质量和化学性质都不变
B.CuO参与反应产生氧气,反应前后质量和化学性质都发生改变
C.CuO是这个反应的催化剂,反应前后质量和化学性质不变
【实验】
步骤1:用试管取少量过氧化氢溶液,将带火星的木条伸入试管中,观察现象.
步骤2:该同学将CuO放在天平的右盘进行称量,左盘的砝码为2g,游码的读数为0.8g.将称好的CuO倒入上述试管中,迅速将带火星的木条伸入试管内,观察现象.
步骤3:待步骤2试管中不再产生气泡,过滤将试管中的固体和液体分离开来,将得到的固体烘干,称量固体的质量.
步骤4:将步骤3得到的固体再加入到过氧化氢溶液中迅速将带火星的木条伸入试管中,观察现象.
(1)填写下表
| 步骤1的现象 | 步骤2的结果 | 步骤4的现象 | 结论 |
| 产生大量气泡,带火星的木条复燃 | 固体的质量为 1.2g | 产生大量气泡,带火星的木条复燃 | 猜想A、B不成立,猜想C成立 |
(3)步骤3的目的是验证氧化铜化学反应前后的质量不变.
(4)请写出该实验的化学反应方程式2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH6.5-8.5,铜<1.0mg•L-1,铁<0.3mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
(2)自来水属于混合物(填“纯净物”或“混合物”); 自来水中的游离氯有少量可转变成氯离子,氯离子的符号是Cl-.
(5)检验水是硬水还是软水,可用的物质是肥皂水,生活中使硬水软化的常用方法是煮沸.
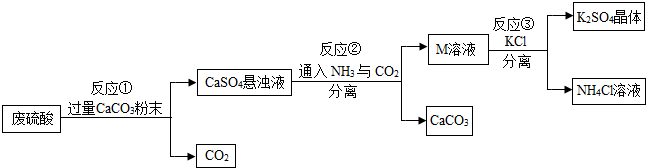
| 物质 | KCL | K2SO4 | NH4Cl | (NH4)2SO4 |
| 溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(2)上述流程中,除可综合利用CO2外,还可循环使用的物质是CaCO3(填写化学式).
(3)反应③中相关物质的溶解度如表所示.反应③在常温下 能实现的原因是常温下K2SO4的溶解度小.
(4)洗涤反应③所得晶体不用水而用饱不用填和K2SO4溶液的目的是减少K2SO4的溶解;
检验此晶体是否洗涤干净的方法是可取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净.
| A. | 金刚石用来切割玻璃 | B. | 用氢气作探究空气球中的气体 | ||
| C. | 乙醇被用作内燃机中的燃料 | D. | 铝用于制造导线 |
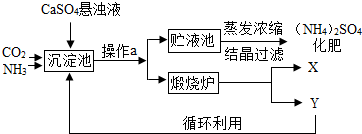 某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.
某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.