题目内容
7.20℃时,100gA物质的不饱和溶液,温度保持不变蒸发掉20g水,有5gA析出,则20℃时,A物质的溶解度为( )| A. | 10g/100g水 | B. | 20g/100g水 | C. | 25g/100g水 | D. | 无法计算 |
分析 20℃时,100gA物质的不饱和溶液,温度保持不变蒸发掉20g水,有5gA析出,说明20g水中溶解了大于5g溶质A,结合溶解度的表达式进行分析.
解答 解:20℃时,100gA物质的不饱和溶液,温度保持不变蒸发掉20g水,有5gA析出,说明20g水中溶解了大于5g溶质A,由于溶液没有饱和,无法计算20℃时,A物质的溶解度.
故选:D.
点评 本题考查了溶解度的计算,题目难度不大,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
11.某化学兴趣小组的同学在探究酸碱的化学性质时,做了如下实验.请你一起与小组同学完成下列探究活动:
【学生实验】取一定质量的澄清石灰水,滴加稀盐酸,无明显现象.请写出反应方程式 ①Ca(OH)2+2HCl=CaCl2+2H2O.
【提出问题】反应后溶液中的溶质成分是什么?
【假设猜想】猜想Ⅰ:溶质为CaCl2; 猜想Ⅱ:CaCl2和HCl;
猜想Ⅲ:②CaCl2和Ca(OH)2; 猜想Ⅳ:CaCl2和Ca(OH)2和HCl;
某同学认为以上猜想有一个是不合理的,是猜想 ③Ⅳ(填序号)并说明原因 ④氢氧化钙和稀盐酸不能共存.
【实验探究】用上述反应后的溶液进行如下实验(填写表格中未完成的项目):
【实验结论】通过以上实验探究,得出猜想⑦Ⅱ成立.
【拓展迁移】小组同学反思了酸碱中和反应如果没有明显现象,通常在反应前的溶液中先滴加酸碱指示剂,借助指示剂颜色的变化来判断反应进行的程度.
下列中和反应需要借助指示剂来判断反应发生的是⑧BD(填字母)
A.氢氧化钡溶液和稀硫酸 B.烧碱溶液和稀硫酸
C.氢氧化铁和稀盐酸 D.氢氧化钾溶液和稀盐酸.
【学生实验】取一定质量的澄清石灰水,滴加稀盐酸,无明显现象.请写出反应方程式 ①Ca(OH)2+2HCl=CaCl2+2H2O.
【提出问题】反应后溶液中的溶质成分是什么?
【假设猜想】猜想Ⅰ:溶质为CaCl2; 猜想Ⅱ:CaCl2和HCl;
猜想Ⅲ:②CaCl2和Ca(OH)2; 猜想Ⅳ:CaCl2和Ca(OH)2和HCl;
某同学认为以上猜想有一个是不合理的,是猜想 ③Ⅳ(填序号)并说明原因 ④氢氧化钙和稀盐酸不能共存.
【实验探究】用上述反应后的溶液进行如下实验(填写表格中未完成的项目):
| 实验方案 | 方案一:加锌粒 | 方案二:滴加酚酞溶液 |
| 实验操作 | 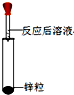 | 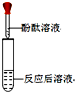 |
| 实验现象 | ⑤产生气泡 | 无明显现象 |
| 实验结论 | 溶液中有HCl | 溶液中无⑥Ca(OH)2 |
【拓展迁移】小组同学反思了酸碱中和反应如果没有明显现象,通常在反应前的溶液中先滴加酸碱指示剂,借助指示剂颜色的变化来判断反应进行的程度.
下列中和反应需要借助指示剂来判断反应发生的是⑧BD(填字母)
A.氢氧化钡溶液和稀硫酸 B.烧碱溶液和稀硫酸
C.氢氧化铁和稀盐酸 D.氢氧化钾溶液和稀盐酸.
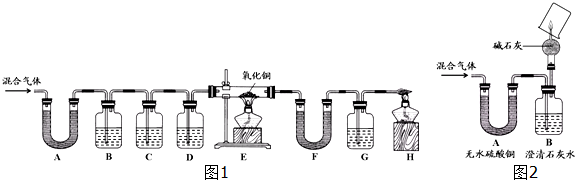
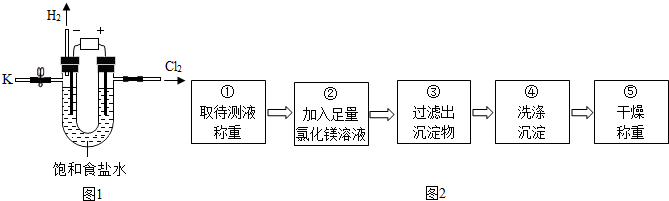
8.某学习小组进行如图1所示电解饱和食盐水的实验.一段时间后,关闭电源,从K处导出一定量的溶液作为待测液进行如下探究.(老师提示:I.电解饱和食盐水的化学方程式:2NaCl+2H2O═2NaOH+H2↑+Cl2↑Ⅱ.忽略其他可能发生的反应对本实验的影响.)
(1)若选用某种酸碱指示剂对待测液进行检验,请你填写表.
(2)甲同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
则氢氧化钠与稀盐酸恰好完全反应时稀盐酸的体积为9.8mL.
(3)乙同学查阅资料发现:氢氧化钠能与氯化镁在溶液中发生反应:
2NaOH+MgCl2═Mg(OH)2↓+2NaCl.
乙同学按如图2实验步骤进行实验:
步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).步骤③过滤出的沉淀物是氢氧化镁,利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”)

(1)若选用某种酸碱指示剂对待测液进行检验,请你填写表.
| 实验步骤 | 实验现象 | 实验结论 |
| 待测液中含有氢氧化钠. |
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
(3)乙同学查阅资料发现:氢氧化钠能与氯化镁在溶液中发生反应:
2NaOH+MgCl2═Mg(OH)2↓+2NaCl.
乙同学按如图2实验步骤进行实验:
步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论).步骤③过滤出的沉淀物是氢氧化镁,利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”)
9.将H2SO4、NaOH、NaCl三种溶液,按pH由大到小顺序排列正确的是( )
| A. | NaOH>H2SO4>NaCl | B. | NaOH>NaCl>H2SO4 | C. | H2SO4>NaCl>NaOH | D. | H2SO4>NaOH>NaCl |
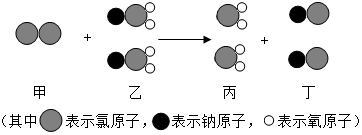 ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒.请回答下列问题:
ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒.请回答下列问题: