题目内容
5.(1)工业上炼铁用一氧化碳还原氧化铁的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.(2)过多的CO2会引起温室效应,绿色植物的光合作用能吸收二氧化碳;科学家发现,以CO2和NH3为原料在高温高压条件下可以合成尿素[化学式是CO(NH2)2],同时会生成水,请写出该反应的化学方程式:CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O;.请你提出一条合理的建议以减缓温室效应:植树造林等(或其他合理答案).
分析 (1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,据此进行分析解答.
(2)根据二氧化碳是绿色植物的光合作用的重要原料,以CO2和NH3为原料在高温高压条件下可以合成尿素[化学式是CO(NH2)2],同时会生成水,结合减缓温室效应的措施,进行分析解答.
解答 解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)过多的CO2会引起温室效应,二氧化碳是绿色植物的光合作用的重要原料,绿色植物的光合作用能吸收二氧化碳.
以CO2和NH3为原料在高温高压条件下可以合成尿素[化学式是CO(NH2)2],同时会生成水,反应的化学方程式为:CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O.
大力
故答案为:(1)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)光合作用;CO2+2NH3$\frac{\underline{\;高温、高压\;}}{\;}$CO(NH2)2+H2O;植树造林等(或其他合理答案).
点评 本题难度不大,掌握工业上用一氧化碳还原氧化铁炼铁的反应原理、自然界的碳循环、化学方程式的书写方法、减缓温室效应的措施等是正确解答本题的关键.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案
相关题目

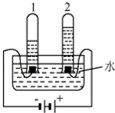 水是一种重要的资源.
水是一种重要的资源.