题目内容
7.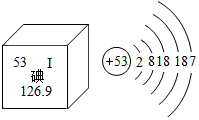 美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖.如图下列关于碘的说法错误的是( )
美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖.如图下列关于碘的说法错误的是( )| A. | 碘的相对原子质量约为126.9g | |
| B. | 碘元素与钙元素形成化合物的化学式为CaI2 | |
| C. | 碘元素与氯元素具有相似的化学性质 | |
| D. | 碘原子的核电荷数=质子数=核外电子数=53 |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;汉字下面的数字表示相对原子质量,进行分析解答即可.根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似;据此进行分析解答.
解答 解:A.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为126.9,没有单位g,故错误.
B.碘原子的最外层有7个电子,易得到1个电子,显-价,钙元素为+2价,碘元素与钙元素形成化合物的化学式为CaI2,故正确;
C.碘原子的最外层有7个电子,氯原子的最外层也是7个电子,最外层电子数相同,因此化学性质相似,故正确;
D.根据元素周期表中的一格可知,左上角的数字为53,表示原子序数为53;根据原子序数=核电荷数=质子数=核外电子数=53,故正确.
故选A.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子结构示意图的含义进行分析解题的能力.

练习册系列答案
相关题目
5.配制稀硫酸的部分操作过如图所示,其中错误的是( )
| A. |  取浓硫酸 | B. |  读取数据 | C. |  稀释 | D. |  装瓶 |
18.除去下列物质中混有的少量杂质(括号内为杂质),所用试剂和方法不正确的是( )
| A. | N2中的(O2 ) 红热的木炭 | |
| B. | NaCl溶液中的(Na2CO3) 加入稀盐酸 | |
| C. | FeCl2溶液中的(CuCl2) 加入过量铁粉,过滤 | |
| D. | 铜粉中的(铁) 加入过量稀硫酸,过滤 |
15.溶液在日常生活中应用广泛.下列对溶液的有关说法正确的是( )
| A. | 溶液都是无色、透明的液体 | |
| B. | 溶液中不能同时存两种溶质 | |
| C. | 溶液中各部分密度不同 | |
| D. | 外界条件不改变,溶质溶剂不会分离 |
12.合金中除含金属外,也可以含有非金属.已知某铝合金粉末除含铝、铜外,还含镁和硅中的一种或两种.小冬设计实验对该铝合金粉末进行探究.
【查阅资料】
(1)硅不能与盐酸反应.
(2)铜、镁不能与氢氧化钠溶液反应
(3)铝、硅能与氢氧化钠溶液反应且得到相同的气体.硅有氢氧化钠的溶液反应的方程式为
Si+2NaOH+H2O=Na2SiO3+2H2↑,足量铝与氢氧化钠溶液反应后溶液的溶质为NaAlO2,则铝与氢氧化钠溶液反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
【提出猜想】
猜想一:该粉末中除含铝、铜外,还含有镁.
猜想二:该粉末中除含铝、铜外,还含有硅.
猜想三:该粉末中除含铝、铜外,还含有镁和硅.
【设计实验】
【实验结论】猜想三正确.
【查阅资料】
(1)硅不能与盐酸反应.
(2)铜、镁不能与氢氧化钠溶液反应
(3)铝、硅能与氢氧化钠溶液反应且得到相同的气体.硅有氢氧化钠的溶液反应的方程式为
Si+2NaOH+H2O=Na2SiO3+2H2↑,足量铝与氢氧化钠溶液反应后溶液的溶质为NaAlO2,则铝与氢氧化钠溶液反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
【提出猜想】
猜想一:该粉末中除含铝、铜外,还含有镁.
猜想二:该粉末中除含铝、铜外,还含有硅.
猜想三:该粉末中除含铝、铜外,还含有镁和硅.
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | ①取一定量的合金粉末,加过量 的稀盐酸,充分反应后过滤 | 粉末部分溶解,并有无色气体放出 | 粉末中还含有硅 |
| ②取步骤①所得滤渣,加过量 的氢氧化钠溶液,充分反应 | 滤渣部分溶解,并有无色气体放出 | ||
| 实验二 | 1、取一定量的合金粉末,加过量NaOH溶液,充分反应后过滤. 2、取滤渣,加盐酸或硫酸 | 略 | 粉末中还含有镁 |
17.下列各物质的化学名称、俗名、化学式以及该物质的分类均正确的是( )
| A. | 碳酸氢钠、苏打、NaHCO3、酸 | B. | 汞、水银、Ag、金属单质 | ||
| C. | 氢氧化钙、石灰水、Ca(OH)2、碱 | D. | 乙醇、酒精、C2H5OH、有机化合物 |


