题目内容
17.将含氧元素质量分数为64%的一氧化碳和二氧化碳的混合气体10g依次通过足量的灼热的氧化铜、澄清的石灰水.完全反应后得到白色沉淀的质量为( )| A. | 10g | B. | 20g | C. | 30g | D. | 无法计算 |
分析 由题意“测得某CO与CO2的混合气体中,氧元素的质量分数为64%”,而碳元素的质量分数为1-64%=36%,则可求该混合气体10g中的碳元素的质量;根据质量守恒定律的元素守恒,“将该混合气体10g通过足量灼热的氧化铜后”,碳元素都会转化为二氧化碳中,则根据二氧化碳与氢氧化钙溶液反应的化学方程式,碳元素都会转化为碳酸钙中,根据碳元素守恒可求碳酸钙的质量.
解答 解:由题意“测得某CO与CO2的混合气体中,氧元素的质量分数为64%”,而碳元素的质量分数为1-64%=36%,则混合气体10g中的碳元素的质量:10g×36%=3.6g;
根据质量守恒定律的元素守恒,将该混合气体10g通过足量灼热的氧化铜后,一氧化碳与氧化铜反应全部转化成二氧化碳,碳元素都会转化为二氧化碳中,所得二氧化碳通入足量的澄清石灰水中,生成碳酸钙沉淀,碳元素又全部转移到碳酸钙中去了.
设最多可得白色沉淀的质量为x.
C~CaCO3↓
12 100
3.6g x
$\frac{12}{3.6g}=\frac{100}{x}$
解得 x=30g.
故选:C.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
7. 硼酸常用于治疗小儿湿疹.如图是硼元素在元素周期表中的相关信息.下列关于硼元素的说法中不正确的是( )
硼酸常用于治疗小儿湿疹.如图是硼元素在元素周期表中的相关信息.下列关于硼元素的说法中不正确的是( )
 硼酸常用于治疗小儿湿疹.如图是硼元素在元素周期表中的相关信息.下列关于硼元素的说法中不正确的是( )
硼酸常用于治疗小儿湿疹.如图是硼元素在元素周期表中的相关信息.下列关于硼元素的说法中不正确的是( )| A. | 元素符号为B | B. | 是非金属元素 | ||
| C. | 原子核外有5个电子 | D. | 相对原子质量为10.81 g |
2.下列变化中与其他三个本质不同的是( )
| A. | 炼铁、炼钢 | B. | 水蒸馏 | C. | 食物腐败变质 | D. | 盐酸除铁锈 |
9.下列物质的名称和俗名对应正确的是( )
| A. | 氢氧化钠一纯碱 | B. | 氢氧化钠一食盐 | C. | 碳酸钠一小苏打 | D. | 氧化钙一生石灰 |
16.在强酸性和强碱性的溶液中都能大量存在的离子是( )
| A. | CO32- | B. | K+ | C. | NH4+ | D. | Cu2+ |

 如图所示,A~H是初中化学常见的物质.A和B可发生中和反应,X常用作食品干燥剂,Y为单质.根据图示回答下列问题:
如图所示,A~H是初中化学常见的物质.A和B可发生中和反应,X常用作食品干燥剂,Y为单质.根据图示回答下列问题: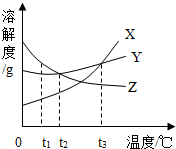 如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.
如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题. .
.