题目内容
6.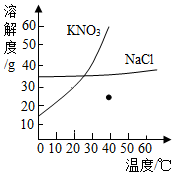 根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题.
根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)(3)将 l00gKNO3跟36gNaCl的混合物放入l00g60℃的水中,充分搅拌,再降温到20℃,有晶体析出,下 列说法中,正确的是BD.
A.60℃时有部分KNO3与溶液共存
B.降温的过程中析出的晶体只有KNO3
C.若要得到更多纯净的硝酸钾晶体可继续降温到0℃
D.20℃时的溶液是NaCl的饱和溶液.
分析 根据表格提供的数据确定溶解度随温度的变化特点进行分析解答;根据析出晶体后的溶液的组成进行分析解答即可.
解答 解:(1)根据表格可以看出,硝酸钾的溶解度随温度的升高而增大明显,故填:硝酸钾;
(2)根据表格可以看出,在40℃时,氯化钠的溶解度为36.6g,故向100g水中加入25g氯化钠固体配制成A溶液,若要使其饱和,至少要再加入36.6g-25g=11.6g氯化钠,故填:11.6;
(3)将 l00gKNO3跟36gNaCl的混合物放入l00g60℃的水中,硝酸钾和氯化钠均全部溶解,降温到20℃,氯化钠恰好饱和,而硝酸钾只能溶解31.6g.故会有固体析出,故填:BD.
点评 本题考查的是溶解度的知识,完成此题,可以依据题干提供的信息结合表格提供的数据进行.

练习册系列答案
相关题目
1.某密闭容器中有X、O2和CO2三种物质,在一定条件下充分反应,测得反应前后各物质的质量如表,请根据表中信息,判断下列说法正确的( )
| 物质 | X | O2 | CO2 | H2O |
| 反应前的质量/g | 23 | 70 | 1 | 0 |
| 反应后的质量/g | 0 | 待测 | 45 | 27 |
| A. | 表中“待测”值为21 | |
| B. | 该反应为分解反应 | |
| C. | X中含有氧元素 | |
| D. | 反应生成的CO2和H2O质量比为45:27 |
14.俗话说:“雷雨发庄稼”,是由于雷雨可给土壤增加( )
| A. | 磷肥 | B. | 氮肥 | C. | 有机肥 | D. | 钾肥 |
18.下列做法是为了隔绝空气中氧气的是( )
| A. | 木制家具表面喷漆 | B. | 油锅着火立即盖上锅盖 | ||
| C. | 澄清石灰水密封保存 | D. | 食品放入冰箱中冷藏 |
15.“经常用脑,多喝六个核桃”,核桃中所含的脂肪主要成分是亚油酸甘油脂(C21H38O4),可供给大脑基质的需要,下列说法正确的是( )
| A. | 亚油酸甘油酯中含有63个原子 | |
| B. | 亚油酸甘油酯中碳、氢的质量比为21:38 | |
| C. | 亚油酸甘油酯中含氢的质量分数最高 | |
| D. | 亚油酸甘油酯属于有机物 |

 A、B、C三种物质的溶解度曲线如图所示,请回答:
A、B、C三种物质的溶解度曲线如图所示,请回答: