题目内容
11.如图1是硝酸钾的溶解度曲线图,某同学在20℃时进行了如图2所示的实验,得到相应的溶液①~⑤,下列说法正确的是( )
| A. | 保持温度不变,若在④中加入4.5KNO3固体可得到饱和溶液 | |
| B. | ②③⑤中溶质的质量分数相等 | |
| C. | ④→⑤可析出53.9gKNO3晶体 | |
| D. | ①③④均为不饱和溶液 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:20℃时硝酸钾的溶解度为31.6g,50℃时硝酸钾的溶解度为85.5g,则20℃时100g水中最多溶解31.6g的硝酸钾,所以
①中加入20g硝酸钾形成的是不饱和溶液;
②中共加入50g硝酸钾不能全部溶解,形成的是该温度下的饱和溶液;
③是升温至50℃,溶质为50g,则为不饱和溶液;
④再加入30g硝酸钾,溶质为80g,是该温度下的不饱和溶液;
⑤降温至20℃溶解度减小,④→⑤可析出晶体的质量=80g-31.6g=48.4g,为20℃时的饱和溶液,所以
A、保持温度不变,50℃时硝酸钾的溶解度为85.5g,即100g水中最多溶解85.5g的硝酸钾,则应加入5.5g,才是饱和溶液,不是4.5 g,故A错误;
B、由以上分析可知:②⑤是20℃时硝酸钾的饱和溶液,溶液的组成相同,溶质的质量分数相等,③中的溶质的质量大,溶质的质量分数大,故B错误;
C、④→⑤可析出晶体的质量=80g-31.6g=48.4g,不是53.9gKNO3晶体,故C错误;
D、①③④均为不饱和溶液,故D正确.
故选:D.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
2.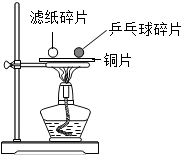 如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )
如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )
 如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )
如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )| A. | 实验说明燃烧的条件之一是温度达到可燃物的着火点 | |
| B. | 铜片受热后变黑,可能是因为产生了氧化铜 | |
| C. | 实验过程中滤纸碎片先燃烧,乒乓球碎片后燃烧 | |
| D. | 实验说明铜有导热性 |
19.金属与我们生活联系密切.
(1)如表是某种常见金属的部分性质:
将该金属投入稀盐酸中,可产生大量的无色气体.根据上述信息回答以下问题:
a.试推断该金属可能的一种用途做导线;
b.该金属的活动性比铜强(填“强”或“弱”);
(2)观察盛水的铁锅,可以发现铁锅与水面接触的一圈最易生锈,其原因是与水接触的地方,同时也与空气接触,在氧气、水的共同作用下,铁最容易生锈,防止铁生锈的措施之一是在铁制品表面刷油漆.
(3)黄铜是由铜锌组成的合金,其颜色与黄金相似.黄铜属于混合物(填“混合物”或“化合物”),有些不法分子将黄铜假冒金元宝骗取钱财,你帮助别人鉴别的方法是(用化学方程式表示):Zn+H2SO4=ZnSO4+H2↑.
(4)a.用盐酸除铁锈Fe2O3+6HCl═2FeCl3+3H2O;
b.烧水的铝壶中常结有一层水垢(水垢的主要成分是CaCO3),用适量的稀盐酸可以将它除去,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑,若盐酸的用量过多,会损坏铝壶,反应的化学方程式是2Al+6HCl═2AlCl3+3H2↑.
(1)如表是某种常见金属的部分性质:
| 颜色、状态 | 硬度 | 密度 | 熔点 | 导电性 | 导热性 | 延展性 |
| 银白色固体 | 较软 | 2.70g/cm3 | 660.4℃ | 良好 | 良好 | 良好 |
a.试推断该金属可能的一种用途做导线;
b.该金属的活动性比铜强(填“强”或“弱”);
(2)观察盛水的铁锅,可以发现铁锅与水面接触的一圈最易生锈,其原因是与水接触的地方,同时也与空气接触,在氧气、水的共同作用下,铁最容易生锈,防止铁生锈的措施之一是在铁制品表面刷油漆.
(3)黄铜是由铜锌组成的合金,其颜色与黄金相似.黄铜属于混合物(填“混合物”或“化合物”),有些不法分子将黄铜假冒金元宝骗取钱财,你帮助别人鉴别的方法是(用化学方程式表示):Zn+H2SO4=ZnSO4+H2↑.
(4)a.用盐酸除铁锈Fe2O3+6HCl═2FeCl3+3H2O;
b.烧水的铝壶中常结有一层水垢(水垢的主要成分是CaCO3),用适量的稀盐酸可以将它除去,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑,若盐酸的用量过多,会损坏铝壶,反应的化学方程式是2Al+6HCl═2AlCl3+3H2↑.
6.下列说法正确的是( )
| A. | 根据质量守恒定律,1 L氢气和1 L氧气反应能生成2 L水 | |
| B. | 蜡烛完全燃烧后,蜡烛没有了,不违背质量守恒定律 | |
| C. | 只有固体、液体间反应遵守质量守恒定律 | |
| D. | 铁在氧气中燃烧,生成四氧化三铁质量等于参加反应的铁丝的质量 |
3.下列有关化学知识的说法正确的是( )
| A. | 铁丝浸没在水中比暴露在潮湿的空气中更容易生锈 | |
| B. | 含氧化全物都是氧化物 | |
| C. | 大多数固体物质的溶解度随温度的升高而增大 | |
| D. | 可燃物只在达到着火点就能燃烧 |
20.如图是某化学反应的微观模拟示意图: 表示氮原子,
表示氮原子, 表示氢原子.下列判断错误的是( )
表示氢原子.下列判断错误的是( )

 表示氮原子,
表示氮原子, 表示氢原子.下列判断错误的是( )
表示氢原子.下列判断错误的是( )
| A. | 该反应遵守质量守恒定律 | |
| B. | 该反应说明化学反应中分子可以再分,原子不可再分 | |
| C. | 化学反应前后A、B、C的分子个数比为1~3~2 | |
| D. | 物质C由一个氮原子和三个氢原子构成 |
1.红曲素是一种食品着色剂的主要成分,其化学式为C21H26O5,下列说法错误的是( )
| A. | 红曲素不属于氧化物 | |
| B. | 红曲素中氢元素的质量分数为$\frac{26}{359}$×100% | |
| C. | 红曲素分子中C、H、O的原子个数之比为21:26:5 | |
| D. | 每个红曲素分子由21个碳原子、26个氢原子和5个氧原子构成 |


