题目内容
5.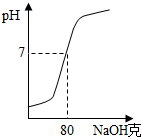 为测定某氢氧化钠溶液的质量分数,现取50g3.65%的稀盐酸,向其中加入此NaOH溶液,所得溶液的pH值与加入NaOH溶液质量的关系如图.则:
为测定某氢氧化钠溶液的质量分数,现取50g3.65%的稀盐酸,向其中加入此NaOH溶液,所得溶液的pH值与加入NaOH溶液质量的关系如图.则:(1)当pH=7时,溶液中的溶质为NaCl(填化学式).
(2)计算该氢氧化钠溶液中溶质的质量分数.
分析 (1)根据图示分析反应的过程以及恰好反应的物质的质量进行分析;
(2)根据反应中消耗的稀盐酸质量可以利用方程式求出氢氧化钠的质量以及氢氧化钠溶液中溶质的质量分数.
解答 解:(1)由曲线情况可知反应过程中,溶液随着氢氧化钠的滴加原溶液的酸性不断变弱,pH不断变大直至两者恰好反应,溶液呈中性溶液的pH=7;从图象可知当加入氢氧化钠溶液的质量为80g时,氢氧化钠和盐酸恰好反应,此时溶液中的溶质是NaCl;
(2)设溶液中氢氧化钠的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
x 50g×3.65%
$\frac{40}{x}$=$\frac{36.5}{50g×3.65%}$
x=2g
氢氧化钠溶液中溶质的质量分数:$\frac{2g}{80g}$×100%=2.5%.
故答案为:(1)NaCl;
(2)氢氧化钠溶液中溶质的质量分数为2.5%.
点评 本题是一道结合图象的计算题,解题时找到PH=7的恰好反应点,并利用化学方程式的计算进行解决是解题的突破口.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
15.下列各组离子能在pH=1的溶液中大量共存,且形成无色溶液的是( )
| A. | Na+ Ba2+Cl-SO42- | B. | Na+CO32-Cl-SO42- | ||
| C. | Cu2+SO42-Na+Cl- | D. | K+SO42-H+Cl- |
16.下列物质中,属于氧化物的是( )
| A. | 水 | B. | 空气 | C. | 乙醇 | D. | 食盐 |
13.下列关于溶液的说法正确的是( )
| A. | 溶液都是均一、稳定的混合物 | |
| B. | 饱和溶液的溶质质量分数一定大于不饱和溶液 | |
| C. | 温度和溶剂的种类不会影响物质的溶解性 | |
| D. | 所有物质溶于水形成溶液都要吸收热量 |
20.甲、乙、丙、丁四种物质在密闭容器中发生化学反应,反应前后各物质的质量变化情况如表所示,则下列说法正确的是( )
| 物质名称 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 10 | 20 | 0 |
| 反应后质量/g | 6 | M | 8 | 26 |
| A. | 甲可能是单质 | B. | 乙、丙、丁是生成物 | ||
| C. | 参加反应的甲、丙质量比为3:4 | D. | 该反应为置换反应 |
10.下列说法错误的是( )
| A. | 增大燃料与空气的接触面积能使燃烧更充分 | |
| B. | 面粉、煤粉等粉尘遇到明火可能发生爆炸 | |
| C. | 釜底抽薪是利用了隔绝空气的灭火原理 | |
| D. | 室内着火需要自救时,可用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区 |

