题目内容
20.甲、乙、丙、丁四种物质在密闭容器中发生化学反应,反应前后各物质的质量变化情况如表所示,则下列说法正确的是( )| 物质名称 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 10 | 20 | 0 |
| 反应后质量/g | 6 | M | 8 | 26 |
| A. | 甲可能是单质 | B. | 乙、丙、丁是生成物 | ||
| C. | 参加反应的甲、丙质量比为3:4 | D. | 该反应为置换反应 |
分析 此题是借助质量守恒定律对反应物生成物先做出判断,再利用质量关系进行求解,反应中反应物质量会减少,生成物质量会增加,从而判断生成物与反应物,即可判断反应的类型,且反应物与生成物质量相等可求出待测的质量,据此回答问题即可.
解答 解:根据质量守恒定律可知,反应前各物质的质量总和=反应后生成各物质的质量总和,则得:20+10+20+0=6+M+8+26,解得M=10.
A、甲、丙的质量减少为反应物,丁的质量增加为生成物,乙的质量不变,肯能是催化剂,也可能不参加反应,因此该反应属于化合反应,故甲可能是单质,故正确;
B、由以上分析可知,甲丙是反应物,丁是生成物,乙可能是催化剂,故错误.
C、参加反应的甲、丙质量比为(20-6):(20-8)=14:12=7:6,故错误;
D、由以上分析,该反应属于化合反应,故错误;
故选A.
点评 本题主要考查了学生根据图表数据分析问题的能力,要学会去伪存真,挖掘出有效数据.然后根据质量守恒定律以及化学反应中的质量关系求解.

练习册系列答案
相关题目
11.向Zn(NO3)2与Cu(NO3)2的混合溶液中加入过量铁粉并过滤.下列说法正确的是( )
| A. | 滤渣中有Zn、Cu、Fe | |
| B. | 滤液中的溶质只有Fe(NO3)2 | |
| C. | 向滤渣中加入稀盐酸会产生气泡 | |
| D. | 反应后滤液的质量比原溶液的质量大 |
15.化学实验中处处表现出颜色变化美.下列化学实验中的颜色变化不符合实验事实的是( )
| A. | 氢氧化钠溶液中滴入石蕊试液,溶液由无色变蓝色 | |
| B. | 铁钉放入硫酸铜溶液中,溶液由蓝色变为浅绿色 | |
| C. | 氢气在空气中燃烧,发出淡蓝色火焰 | |
| D. | 加热玻璃管中的铜粉,固体由红色变成黑色 |
12.下列化学反应不属于置换反应的是( )
| A. | 2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+2Fe | B. | Zn+2HCl═ZnCl2+H2↑ | ||
| C. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | D. | Cu+2AgNO3═2Ag+Cu(NO3)2 |
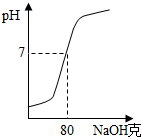 为测定某氢氧化钠溶液的质量分数,现取50g3.65%的稀盐酸,向其中加入此NaOH溶液,所得溶液的pH值与加入NaOH溶液质量的关系如图.则:
为测定某氢氧化钠溶液的质量分数,现取50g3.65%的稀盐酸,向其中加入此NaOH溶液,所得溶液的pH值与加入NaOH溶液质量的关系如图.则: