题目内容
12.家庭里常有食盐、纯碱、食醋、矿泉水、酱油、肥皂等物质.下表列出了家庭中部分物质的近似pH:| 物质 | 食盐水 | 肥皂水 | 食醋 | 酱油 |
| PH | 7 | 10 | 3 | 5 |
(2)如果只可用家里的上述物质,你认为用食醋可区分食盐和纯碱.
(3)蚊虫叮咬人时会分泌出蚁酸,引起肿痒,涂上表中的肥皂水可止痒.
分析 (1)当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性.
(2)根据食盐和纯碱中阴离子的不同进行分析解答.
(3)被蚊虫叮咬后会痒痛是因为蚊虫分泌甲酸,所以应涂抹碱性物质.
解答 解:(1)当溶液的pH大于7时,呈碱性,肥皂水的pH等于10,呈碱性,故填:肥皂水;
(2)纯碱是碳酸钠,食盐的主要成分是氯化钠,碳酸根离子与酸反应会生成二氧化碳气体,食醋中含有醋酸,故可以分别加入食醋,出现气泡的是纯碱,无明显现象的是食盐.故填:食醋;
(3)蚁酸是一种酸,所以可以涂抹弱碱性的物质进行中和;肥皂水的pH为10,大于7,显碱性,可与蚁酸发生中和反应,故填:肥皂水.
点评 本题难度不大,考查同学们灵活运用所学知识进行解题的能力,掌握溶液的酸碱性和溶液pH大小之间的关系、中和反应等是顺利解题的关键.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
2.逻辑推理是学习化学常用的思维方法,下列说法正确的是( )
| A. | 化学反应通常伴有能量变化,凡是伴有能量变化的不一定是化学变化 | |
| B. | 单质中只含有一种元素,则只含有一种元素的物质一定是单质 | |
| C. | 化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物 | |
| D. | 一定温度下的不饱和溶液还能溶解溶质,则一定温度下的饱和溶液不能溶解任何物质 |
3.食醋里含有醋酸,人的胃液里含有盐酸,柠檬、柑橘等水果中含有柠檬酸.这些酸在水中能电离出的共同离子是( )
| A. | Na+ | B. | H+ | C. | OH- | D. | Cl- |
20.下列反应既不属于化合反应,也不属于分解反应的是( )
| A. | 水→氢气+氧气 | B. | 木炭+氧化铜→铜+二氧化碳 | ||
| C. | 氢气+氧气→水 | D. | 氧化汞→汞+氧气 |
7.请将有关物质名称或化学式填在下表空格内:
| 物质名称 | 食盐 | 硫酸亚铁 | 熟石灰 | 硝酸 | 硫酸铝 |
| 化学式 | NaCl | FeSO4 | Ca(OH)2 | HNO3 | Al2(SO4)3 |
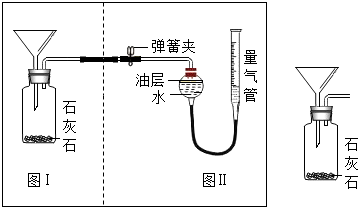 石灰石是一种重要矿石,其主要成分为碳酸钙,在冶金、建材、化工等行业均有广泛用途.某校9年级科学探究小组的同学为了测定某种石灰石样品中碳酸钙的质量分数,设计了如下实验方案:取一定质量的石灰石样品与足量稀盐酸反应,测量反应后生成的CO2的体积,再将体积换算成质量,最后根据CO2的质量计算样品中碳酸钙的质量分数.下图Ⅰ为石灰石与稀盐酸反应的装置,图Ⅱ为测量CO2体积的装置.
石灰石是一种重要矿石,其主要成分为碳酸钙,在冶金、建材、化工等行业均有广泛用途.某校9年级科学探究小组的同学为了测定某种石灰石样品中碳酸钙的质量分数,设计了如下实验方案:取一定质量的石灰石样品与足量稀盐酸反应,测量反应后生成的CO2的体积,再将体积换算成质量,最后根据CO2的质量计算样品中碳酸钙的质量分数.下图Ⅰ为石灰石与稀盐酸反应的装置,图Ⅱ为测量CO2体积的装置.