题目内容
 取三支注射器,编号A、B、C.A中装氢氧化钠溶液,B中装澄清石灰水,C中装稀盐酸,如图所示装置,按以下步骤进行实验:
取三支注射器,编号A、B、C.A中装氢氧化钠溶液,B中装澄清石灰水,C中装稀盐酸,如图所示装置,按以下步骤进行实验:①用A向锥形瓶内注入氢氧化钠溶液,振荡,溶液无明显变化;
②换B抽取锥形瓶内的气体,石灰水没有变化;
③换C向锥形瓶内滴加稀盐酸,开始没有气泡,过一会产生大量气泡;
④换B抽取锥形瓶内的气体,石灰水变浑浊.
(1)写出锥形瓶内发生的一个化学反应方程式
(2)描述气球在实验过程中是如何变化的
(3)滴加稀盐酸刚开始没有气泡产生,推测一个可能的原因
考点:碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:根据已有的知识进行分析,二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,碳酸钠与稀盐酸反应生成二氧化碳、氯化钠和水,二氧化碳能使澄清的石灰水变浑浊.
解答:解:(1)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,碳酸钠与稀盐酸反应生成二氧化碳、氯化钠和水;
(2)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,锥形瓶内压强减小,因此步骤①中气球迅速鼓起并胀大;碳酸钠与稀盐酸反应生成二氧化碳、氯化钠和水,锥形瓶内压强增大,因此③中气球逐渐变瘪;
(3)若步骤①中滴加的氢氧化钠溶液过量,则滴加稀盐酸时,稀盐酸先与氢氧化钠溶液反应,再与碳酸钠反应,因此刚开始没有气泡产生.
故填:(1)CO2+2NaOH=Na2CO3+H2O(或Na2CO3+2HCl=2NaCl+H2O+CO2↑);(2)步骤①中气球迅速鼓起并胀大,③中气球逐渐变瘪;(3)步骤①中滴加的氢氧化钠溶液过量,则滴加稀盐酸时,稀盐酸先与氢氧化钠溶液反应,再与碳酸钠反应.
(2)二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,锥形瓶内压强减小,因此步骤①中气球迅速鼓起并胀大;碳酸钠与稀盐酸反应生成二氧化碳、氯化钠和水,锥形瓶内压强增大,因此③中气球逐渐变瘪;
(3)若步骤①中滴加的氢氧化钠溶液过量,则滴加稀盐酸时,稀盐酸先与氢氧化钠溶液反应,再与碳酸钠反应,因此刚开始没有气泡产生.
故填:(1)CO2+2NaOH=Na2CO3+H2O(或Na2CO3+2HCl=2NaCl+H2O+CO2↑);(2)步骤①中气球迅速鼓起并胀大,③中气球逐渐变瘪;(3)步骤①中滴加的氢氧化钠溶液过量,则滴加稀盐酸时,稀盐酸先与氢氧化钠溶液反应,再与碳酸钠反应.
点评:此题难度较大,掌握该实验的过程并结合氢氧化钠与盐酸的化学性质是顺利结题的关键.

练习册系列答案
相关题目
“以崇尚科学为荣,以愚昧无知为耻”.下列叙述缺乏科学依据的是( )
| A、不可用工业酒精勾兑饮用酒 |
| B、小孩经常咬铅笔芯,会导致铅中毒 |
| C、加碘食盐的“碘”是指碘元素 |
| D、碳酸钙可用作补钙剂 |
下列变化属于化学变化的是( )
| A、冰雪消融 | B、灯泡发光 |
| C、铁钉生锈 | D、铁水铸成锅 |

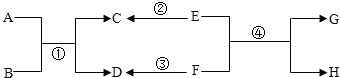 A、B、C、D、E、F、G、H之间的相互转化关系如图,它们均是初中化学中常见的物质,其中B、C是气体,且B是单质,E是含钠元素的化合物,G是一种常见的不溶于水的建筑材料.C、D在一定条件下也能反应生成A和B.
A、B、C、D、E、F、G、H之间的相互转化关系如图,它们均是初中化学中常见的物质,其中B、C是气体,且B是单质,E是含钠元素的化合物,G是一种常见的不溶于水的建筑材料.C、D在一定条件下也能反应生成A和B.

