题目内容
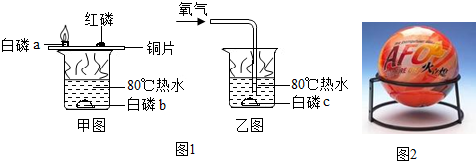
7.随着汽车数量的剧增,下列问题已成为汽车行业研究的新课题(1)能源问题:①汽车最理想的清洁燃料是氢气,这是因为氢气在氧气中点燃后放出的热量大,且生成物为水,无污染;.
②一种新型的“绿色电池-燃料电池”是把H2、CO、CH4等燃料和空气不断输入,直接氧化,使化学能转化为电能,被称为“21世纪的绿色发电站”,这三种气体可以作为燃料的原因为B
A、都是无毒无害的气体 B、都可以燃烧,放出大量的热
C、燃烧产物均为二氧化碳和水 D、均在自然界中大量存在
(2)环境与健康问题:①2010年4月22日是第41个世界地球日.地球日主题为:“珍惜地球资源、转变发展方式、倡导低碳生活”. 保护地球是我们每个公民应尽的义务和责任,下列举措不符合这一主题的是D
A.某些工业废水处理后可循环使用
B.积极开发使用风能、太阳能等新能源,减少化石燃料的使用
C.禁止秸秆就地焚烧,提倡用秸秆代替煤作燃料进行火力发电
D.为减少大气污染,火力发电厂应采取加高烟囟的办法
②市售的补钙药品中含有一定量很细的碳酸钙粉末,食用这样的药品后后,在胃里(胃液中含有盐酸)会被溶解而吸收的原因(化学方程式)是CaCO3+2HCl═CaCl2+H2O+CO2↑.
分析 (1)①根据氢气的燃烧值与生成物回答;
②氢气、一氧化碳、甲烷等物质都具有可燃性,燃烧是能够放出大量的热,常常用作燃料;
(2)①本题可从绿色环保的含义进行分析,只要是保护水资源,保护空气不受污染,节约能源的举措都是正确的.
②根据胃液的成分及盐酸的性质回答.
解答 解:(1)①因为氢气在氧气中点燃后放出的热量大,且生成物为水,无污染,所以汽车最理想的清洁燃料是氢气;
故答案为:氢气在氧气中点燃后放出的热量大,且生成物为水,无污染;
②无毒无害气体不一定能够用作燃料,例如氮气无毒无害,不能用作燃料;氢气燃烧不能生成二氧化碳,一氧化碳燃烧不能生成水;在自然界大量存在的物质不一定能够用作燃料,例如水在自然界大量存在,不能用作燃料.主要是它们都可以燃烧并放出大量的热,可以用作燃料.
故答案为:B;
(2)①工业废水经处理后可以循环使用,以节约水资源,从而保护地球;积极开发使用风能、太阳能、潮汐能等新能源,减少化石燃料的使用可以防止环境污染,从而保护地球;禁止秸秆就地焚烧,提倡用秸秆代替煤作燃料进行火力发电可以减缓环境污染.只有加高烟囟的办法不会减少大气污染.
故答案为:D;
②胃液的成分主要是盐酸,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;.
点评 化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,是中考热点之一,在学习过程中要理论联系实际,在实践中领会知识,运用所学知识去解决实际问题.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
18.写出下列反应的化学方程式,并简答.
| 化学反应 | 化学方程式 | 简答 |
| 煅烧石灰石 | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | 反应类型为分解反应 |
| 铁丝在氧气中燃烧 | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | 生成物颜色为黑色 |
| 碳和氧化铜在高温下反应 | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | 该反应中氧化剂为氧化铜 |
| 二氧化碳通入足量的澄清石灰水 | CO2+Ca(OH)2═CaCO3↓+H2O | 此反应可鉴定二氧化碳 |
2.化学知识中有很多的“相等”.下列叙述正确的是( )
| A. | 原子中原子核内的质子数和中子数一定相等 | |
| B. | 同种元素的原子和离子(如钠原子和钠离子)核外电子数相等 | |
| C. | 化学反应前后各物质的物质总和一定相等 | |
| D. | 溶液稀释前后溶质的质量一定相等 |
12.如图实验基本操作错误的是( )
| A. |  加热液体 | B. |  稀释浓硫酸 | ||
| C. |  测定溶液pH | D. |  向试管内倾倒液体 |
19.某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:氢气也有一氧化碳相似的化学性质3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:得到数据如表:
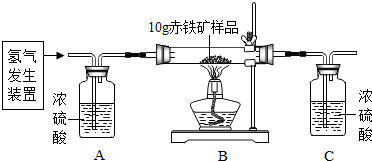
(1)实验前先通一会氢气原因排出装置内的空气,防止加热时产生爆炸;试验中观察到的实验现象为红色粉末变黑;实验结束时先停止加热后停止通入氢气,原因防止生成的铁被氧化.
(2)请计算该赤铁矿石样品中氧化铁的质量分数.80%
(3)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为[(296.8g-294.1g)-(84.3g-81.9g)]:(84.3g-81.9g)(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会不变(选填“偏大”、“偏小”或“不变”).

| 装置 | B | C |
| 反应前质量 | 84.3g | 294.1g |
| 反应后质量 | 81.9g | 296.8g |
(2)请计算该赤铁矿石样品中氧化铁的质量分数.80%
(3)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为[(296.8g-294.1g)-(84.3g-81.9g)]:(84.3g-81.9g)(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会不变(选填“偏大”、“偏小”或“不变”).
10.A、B、C、D四种物质各10克,放入密闭容器中,一定条件下充分反应后,称量,A为12克,B的质量未知,C为6克,D的质量大于10克,则关于A、B、C、D的说法正确的是( )
| A. | A、B是反应物,C、D是生成物 | |
| B. | B可能是催化剂,A、D一定是生成物 | |
| C. | 反应过程中,当容器中C的质量为8克时,D的质量为6克 | |
| D. | 反应结束后经检验B不存在,则容器中D的质量为22克 |
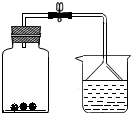 如图所示,向盛有红棕色二氧化氮(NO2)气体的集气瓶中投入几小块木炭或活性炭,最终观察到集气瓶内红棕色消失(填“变深”、“不变”或“消失”),漏斗中液面上升(填“上升”、“下降”或“不变”).其原因是:活性炭有吸附 作用,使瓶中气体压强小于外界大气压(填“大于”、“等于”或“小于”).根据木炭或活性炭的这一性质,写出其在生产、生活中的一种用途制糖工业中作脱色剂(或防毒面具里作滤毒剂等).
如图所示,向盛有红棕色二氧化氮(NO2)气体的集气瓶中投入几小块木炭或活性炭,最终观察到集气瓶内红棕色消失(填“变深”、“不变”或“消失”),漏斗中液面上升(填“上升”、“下降”或“不变”).其原因是:活性炭有吸附 作用,使瓶中气体压强小于外界大气压(填“大于”、“等于”或“小于”).根据木炭或活性炭的这一性质,写出其在生产、生活中的一种用途制糖工业中作脱色剂(或防毒面具里作滤毒剂等).