题目内容
10. 水与人类的生活和生产密切相关.请回答以下问题:
水与人类的生活和生产密切相关.请回答以下问题:(1)生理盐水中的溶剂是水.
(2)保护水环境、珍爱水资源,是每个公民应尽的责任和义务.下列做法有利于保护水资源的是B(填序号).
A.大量使用化肥农药
B.工业废水处理达标后排放
C.使用含磷洗衣粉
D.生活污水直接排放
(3)在水蒸发的过程中,下列说法正确的是A(填序号).
A.水分子不断运动
B.水分子之间间隔不变
C.水分子分解成氢原子和氧原子
D.水分子可以保持水的物理性质
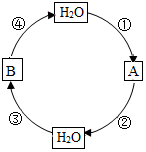
(4)课外活动中,同学们玩起了以水为主题的“化学反应接龙”游戏.游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环,如图所示.仿照示例完成下列反应的化学方程式.
示例:①分解反应:电解水2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
②置换反应H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu;
③化合反应CaO+H2O═Ca(OH)2;
④复分解反应Ca(OH)2+2HCl═CaCl2+2H2O.
分析 根据溶液的成分、保护水资源的措施、水蒸发的微观实质以及化学方程式的书写进行分析解答即可.
解答 解:(1)生理盐水中的溶剂是水,故填:水.
(2)A.大量使用化肥农药会造成水体污染;
B.工业废水处理达标后排放能保护水资源;
C.使用含磷洗衣粉会造成水污染;
D.生活污水直接排放会造成水污染;
故填:B;
(3)在水蒸发的过程中水分子不断运动,水分子之间间隔变大,水分子不变,水分子可以保持水的化学性质,故填:A;
(4)②氢气和氧化铜加热生成水和铜,是置换反应,故填:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu;
③氧化钙与水反应生成氢氧化钙,是化合反应,故填:CaO+H2O═Ca(OH)2;
④氢氧化钙与盐酸反应生成氯化钙和水,是复分解反应,故填:Ca(OH)2+2HCl═CaCl2+2H2O.
点评 本题考查的是水资源的知识以及化学方程式的书写,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
20.小明同学对所学部分化学知识归纳如下,其中完全正确的一组是( )
| A.物质的分类 | B.用“化学”眼光分析 |
| ①玻璃、塑料都属于无机非金属材料 ②含碳的化合物都属于有机物 ③涤纶、羊毛和棉花属于天然纤维 | ①工业制汽水时,利用 加压的方法使大量的二氧化碳气体溶解在水里 ②地里庄稼出现叶色发黄需施用氮肥 ③装食品用的聚乙烯塑料袋可以通过加热进行封口 |
| C.“元素与健康”的关系 | D.物质的俗称、学名与化学式 |
| ①做菜时用铁强化酱油调味防治贫血 ②大米给人体提供的营养素是蛋白质 ③氟、铁、钠是人体所需的微量元素 | ①酒精 乙醇 C2H6O ②盐酸 氢氯酸 HCl ③铜绿 氢氧化铜 Cu2(OH)2CO3 |
| A. | A | B. | B | C. | C | D. | D |
18.小亮同学想通过实验探究某企业采用的氨碱法制得纯碱样品的成分及含量.
【提出问题1】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,小亮做出如下假设:
①只含有Na2CO3;②含有Na2CO3和NaHCO3
【查阅资料】
(1)表中的现象I对应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑
(2)现象Ⅱ为有白色沉淀产生.
【实验探究】为了确定纯碱样品的成分,小亮设计如下实验方案,请你一起完成下列实验报告.
【实验反思】实验步骤①中,氯化钙溶液过量的目的是将碳酸钠全部除去
【提出问题2】如何测量该纯碱样品中各物质的含量?
(1)为测量该纯碱样品各成分的含量,小亮设计了如图1装置,通过称量B装置的质量变化来 确定样品中各成分的含量.该装置气密性良好,稀硫酸与样品、进人装置B的C02与NaOH 均完全反应,操作无误,但多次实验发现,测定结果有偏差.造成偏差的原因有①空气中的CO2进入装置B被氢氧化钠吸收;②装置A中残留的CO2未被装置B中的氢氧化钠吸收.
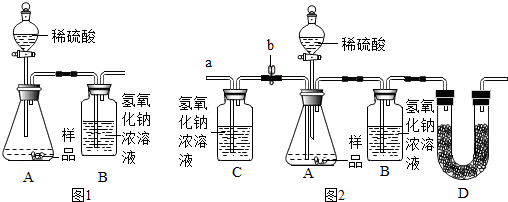
(2)小亮在老师的指导下重新设计了如图2所示的实验装置.该实验有以下操作步骤:
①检查装置气密性,将干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
⑥打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
⑦根据B瓶增加的质量,计算样品中各成分的含量.
该实验的正确步骤是①③②④⑥⑤⑦.
【提出问题1】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,小亮做出如下假设:
①只含有Na2CO3;②含有Na2CO3和NaHCO3
【查阅资料】
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
(2)现象Ⅱ为有白色沉淀产生.
【实验探究】为了确定纯碱样品的成分,小亮设计如下实验方案,请你一起完成下列实验报告.
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量 的CaCl2溶液. | 有白色沉淀产生 | 该反应的方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ②将上述反应后的混合液过滤,取滤液. | 有气泡冒出 | 证明猜想②成立. |
【提出问题2】如何测量该纯碱样品中各物质的含量?
(1)为测量该纯碱样品各成分的含量,小亮设计了如图1装置,通过称量B装置的质量变化来 确定样品中各成分的含量.该装置气密性良好,稀硫酸与样品、进人装置B的C02与NaOH 均完全反应,操作无误,但多次实验发现,测定结果有偏差.造成偏差的原因有①空气中的CO2进入装置B被氢氧化钠吸收;②装置A中残留的CO2未被装置B中的氢氧化钠吸收.

(2)小亮在老师的指导下重新设计了如图2所示的实验装置.该实验有以下操作步骤:
①检查装置气密性,将干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
⑥打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
⑦根据B瓶增加的质量,计算样品中各成分的含量.
该实验的正确步骤是①③②④⑥⑤⑦.


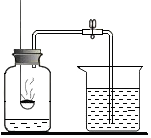 在“空气中氧气含量的测定”实验探究中,(实验装置如图所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,(实验装置如图所示)回答下列问题: 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格:
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格: