题目内容
某兴趣小组的同学对一包在空气中敞口放置一段时间的碱石灰产生了好奇,于是他们对这包碱石灰的成分展开了探究.
【提出问题】他们要探究的问题是 .
【查阅资料】
①碱石灰是由CaO与NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体;
②熟石灰固体溶解度小,溶于水放出的热量少,可以忽略不计.
【提出猜想】该碱石灰的主要成分可能含有CaO、NaOH、Ca(OH)2、CaCO3和 .
【实验探究】小组的同学设计实验并进行验证,过程如下:
①小明取部分该碱石灰样品于试管中,加少量水后无放热现象,说明这包碱石灰样品中不含 ,继续加足量水,振荡、静置后有白色沉淀,小明认为碱石灰样品中一定含有CaCO3,小美认为他的结论不准确,原因是: .(用化学方程式表示)
②从小明的试管中取少量上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成.
③把过程②所得物质过滤,向滤液中滴加无色酚酞溶液,溶液变红色.
【解释与结论】根据 以上探究:
①你认为该包碱石灰样品一定含有的物质是 ,可能含有的物质是 .
②实验探究过程. ③所得溶液中除酚酞外还含有的溶质是 .
【迁移应用】
下列气体:①氢气 ②氧气 ③一氧化碳 ④氯化氢 ⑤二氧化硫 ⑥氨气,不能用碱石灰干燥的是 (填字母序号).
A、①②③B、④⑤⑥C、④⑤D、⑤⑥
【提出问题】他们要探究的问题是
【查阅资料】
①碱石灰是由CaO与NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体;
②熟石灰固体溶解度小,溶于水放出的热量少,可以忽略不计.
【提出猜想】该碱石灰的主要成分可能含有CaO、NaOH、Ca(OH)2、CaCO3和
【实验探究】小组的同学设计实验并进行验证,过程如下:
①小明取部分该碱石灰样品于试管中,加少量水后无放热现象,说明这包碱石灰样品中不含
②从小明的试管中取少量上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成.
③把过程②所得物质过滤,向滤液中滴加无色酚酞溶液,溶液变红色.
【解释与结论】根据 以上探究:
①你认为该包碱石灰样品一定含有的物质是
②实验探究过程. ③所得溶液中除酚酞外还含有的溶质是
【迁移应用】
下列气体:①氢气 ②氧气 ③一氧化碳 ④氯化氢 ⑤二氧化硫 ⑥氨气,不能用碱石灰干燥的是
A、①②③B、④⑤⑥C、④⑤D、⑤⑥
考点:实验探究物质的组成成分以及含量,生石灰的性质与用途,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【提出问题】根据猜想可知要探究的问题是这包久置的碱石灰样品的成分是什么进行解答;
【提出猜想】氧化钙和水反应生成氢氧化钙,氢氧化钙易吸收空气中二氧化碳生成碳酸钙,二氧化碳和氢氧化钠反应生成碳酸钠和水由此解答;
【实验探究】①根据氧化钙和水反应生成氢氧化钙,且放出大量的热,氢氧化钠固体溶解也会放出大量热;氢氧化钙和碳酸钠溶液反应碳酸钙沉淀和氢氧化钠进行解答;
【解释与结论】①根据碳酸钠溶液能和氯化钡溶液反应生成碳酸钡沉淀和氯化钠,氢氧化钠溶液呈碱性,能使酚酞试液变红进行解答;
②根据氢氧化钠溶液呈碱性,能使酚酞试液变红以及氯化钡溶液过量进行解答;
【迁移应用】根据能和碱石灰反应的气体不能用碱石灰干燥进行解答.
【提出猜想】氧化钙和水反应生成氢氧化钙,氢氧化钙易吸收空气中二氧化碳生成碳酸钙,二氧化碳和氢氧化钠反应生成碳酸钠和水由此解答;
【实验探究】①根据氧化钙和水反应生成氢氧化钙,且放出大量的热,氢氧化钠固体溶解也会放出大量热;氢氧化钙和碳酸钠溶液反应碳酸钙沉淀和氢氧化钠进行解答;
【解释与结论】①根据碳酸钠溶液能和氯化钡溶液反应生成碳酸钡沉淀和氯化钠,氢氧化钠溶液呈碱性,能使酚酞试液变红进行解答;
②根据氢氧化钠溶液呈碱性,能使酚酞试液变红以及氯化钡溶液过量进行解答;
【迁移应用】根据能和碱石灰反应的气体不能用碱石灰干燥进行解答.
解答:解:【提出问题】根据猜想可知要探究的问题是这包久置的碱石灰样品的成分是什么;故填:这包久置的碱石灰样品的成分是什么;
【提出猜想】氧化钙和水反应生成氢氧化钙,氢氧化钙易吸收空气中二氧化碳生成碳酸钙,二氧化碳和氢氧化钠反应生成碳酸钠和水,所以该碱石灰的主要成分可能含有CaO、Ca(OH)2、CaCO3、NaOH和Na2CO3;故填:Na2CO3;
【实验探究】①氧化钙和水反应生成氢氧化钙,且放出大量的热,氢氧化钠固体溶解也会放出大量热,所以加少量水后无放热现象,说明这包碱石灰样品中不含氧化钙和氢氧化钠;氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以不一定含有碳酸钙,化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;故填:CaO、NaOH;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
【解释与结论】①碳酸钠溶液能和氯化钡溶液反应生成碳酸钡沉淀和氯化钠,所以取少量上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成,说明一定含有碳酸钠;②过滤后所得物质能使酚酞试液变红,说明有氢氧化钠(此时溶液中不可能有氢氧化钙,因为有碳酸钠),又因为原固体混合物中没有NaOH,所以应该是Ca(OH)2和Na2CO3反应生成了NaOH,因此固体混合物中一定有Ca(OH)2;
故填:Na2CO3、Ca(OH)2;CaCO3;
②氢氧化钠溶液呈碱性,能使酚酞试液变红以及氯化钡溶液过量,所以③所得溶液中除酚酞外还含有的溶质是氢氧化钠、氯化钠和氯化钡;故填:NaOH、NaCl、BaCl2;故填:NaOH、NaCl、BaCl2;
【迁移应用】能和碱石灰反应的气体不能用碱石灰干燥,其中氯化氢和二氧化硫能和氢氧化钠,所以不能用碱石灰干燥.故选:C.
【提出猜想】氧化钙和水反应生成氢氧化钙,氢氧化钙易吸收空气中二氧化碳生成碳酸钙,二氧化碳和氢氧化钠反应生成碳酸钠和水,所以该碱石灰的主要成分可能含有CaO、Ca(OH)2、CaCO3、NaOH和Na2CO3;故填:Na2CO3;
【实验探究】①氧化钙和水反应生成氢氧化钙,且放出大量的热,氢氧化钠固体溶解也会放出大量热,所以加少量水后无放热现象,说明这包碱石灰样品中不含氧化钙和氢氧化钠;氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以不一定含有碳酸钙,化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;故填:CaO、NaOH;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
【解释与结论】①碳酸钠溶液能和氯化钡溶液反应生成碳酸钡沉淀和氯化钠,所以取少量上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成,说明一定含有碳酸钠;②过滤后所得物质能使酚酞试液变红,说明有氢氧化钠(此时溶液中不可能有氢氧化钙,因为有碳酸钠),又因为原固体混合物中没有NaOH,所以应该是Ca(OH)2和Na2CO3反应生成了NaOH,因此固体混合物中一定有Ca(OH)2;
故填:Na2CO3、Ca(OH)2;CaCO3;
②氢氧化钠溶液呈碱性,能使酚酞试液变红以及氯化钡溶液过量,所以③所得溶液中除酚酞外还含有的溶质是氢氧化钠、氯化钠和氯化钡;故填:NaOH、NaCl、BaCl2;故填:NaOH、NaCl、BaCl2;
【迁移应用】能和碱石灰反应的气体不能用碱石灰干燥,其中氯化氢和二氧化硫能和氢氧化钠,所以不能用碱石灰干燥.故选:C.
点评:题以生活中常见的食品干燥剂为情境角度出发,考查干燥剂是否变质的实验探究的综合性推断题,考查了CO2、NaOH、Ca(OH )2、CaCO3 之间如何相互转化,特别是考查学生的在实验探究中推断分析能力,和平时对含碳的化合物的化学性质的积累!通过该实验探究结果引发学生在化学实验室中氢氧化钙如何正确保存,做到学以致用.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
青少年过多摄入蛋糕里的人造奶油会产生一种影响身体发育的反式脂肪酸,其化学式为C18H34O2.下列对该物质的说法中不正确的是( )
| A、氢元素的质量分数是12.06% |
| B、由碳、氢、氧三种元素组成 |
| C、由54个原子构成 |
| D、碳元素与氧元素的原子个数比为9:1 |
 有一种市场上常见的食用加碘盐,其包装袋上部分标签如图所示,试回答下列问题:
有一种市场上常见的食用加碘盐,其包装袋上部分标签如图所示,试回答下列问题:

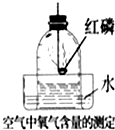 用红磷在钟罩中燃烧来测定空气中氧气的含量,发生的实验现象是:
用红磷在钟罩中燃烧来测定空气中氧气的含量,发生的实验现象是: