题目内容
9.在Cu(NO3)2、Mg(NO3)2和AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体上滴加稀盐酸时有气泡产生,则反应后所得溶液中含有的金属离子有镁离子和亚铁离子;滤出的固体中含有的金属是银、铜和铁.分析 镁比铁活泼,铁比铜活泼,铜比银活泼;
铜和银不能和稀盐酸反应,铁能和稀盐酸反应生成氯化亚铁和氢气.
解答 解:镁比铁活泼,因此铁不能和硝酸镁反应;
铁能和硝酸铜反应生成硝酸亚铁和铜,能和硝酸银反应生成硝酸亚铁和银,向滤出的固体上滴加稀盐酸时有气泡产生,说明滤出的固体中含有铁,即反应过程中铁是过量的,因此反应后所得溶液中含有的金属离子有镁离子和反应生成的亚铁离子;
滤出的固体中含有的金属有过量的铁和生成的铜和银.
故填:镁离子和亚铁离子;银、铜和铁.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19. 某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
【提出问题】溶液为什么会变红呢?
【查阅资料】过氧化钠与水发生了化学反应,生成碱性物质,碱性物质能使酚酞试液变红.
【猜想假设】甲同学认为生成了碳酸钠; 乙同学认为生成了氢氧化钠.
【实验探究】
(1)小明认为甲同学的猜想无需验证就知道是错误的.他的理由是反应物中不含有碳元素,因此不能生成碳酸钠.
(2)为了证实小明的看法,小组设计了一个证明碳酸钠不存在并验证生成物的实验.
【得出结论】根据实验分析,过氧化钠与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
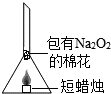
【拓展反思】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气.小红同学又设计了一个如图所示实验(蜡烛火焰与棉花不接触).请回答:
(1)棉花能(填“能”或“不能”)燃烧,这主要是因为蜡烛燃烧生成了能与过氧化钠反应的物质水和二氧化碳,同时反应放热.
(2)结合上述实验事实,请你对运输过氧化钠固体过程中提出一条安全建议:密封保存.
 某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.
某化学兴趣小组同学用实验室中的过氧化钠(Na2O2)粉末进行实验,取少量粉末放入试管中并加入水,观察到有气泡产生,用带火星的木条放在试管口,木条复燃,则该气体是氧气;另取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红.【提出问题】溶液为什么会变红呢?
【查阅资料】过氧化钠与水发生了化学反应,生成碱性物质,碱性物质能使酚酞试液变红.
【猜想假设】甲同学认为生成了碳酸钠; 乙同学认为生成了氢氧化钠.
【实验探究】
(1)小明认为甲同学的猜想无需验证就知道是错误的.他的理由是反应物中不含有碳元素,因此不能生成碳酸钠.
(2)为了证实小明的看法,小组设计了一个证明碳酸钠不存在并验证生成物的实验.
| 实验操作 | 实验现象 | 实验结论 |
| 取过氧化钠与水反应后的溶液放入试管中,向其中滴加足量稀盐酸. | 无气泡产生 | 不存在碳酸钠 |
| 另取过氧化钠与水反应后的溶液放入试管中,向其中滴加硫酸铜溶液. | 产生蓝色沉淀 | 乙猜想正确 |
【拓展反思】过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气.小红同学又设计了一个如图所示实验(蜡烛火焰与棉花不接触).请回答:
(1)棉花能(填“能”或“不能”)燃烧,这主要是因为蜡烛燃烧生成了能与过氧化钠反应的物质水和二氧化碳,同时反应放热.
(2)结合上述实验事实,请你对运输过氧化钠固体过程中提出一条安全建议:密封保存.
20.下列有关溶液的说法符合实际的是( )
| A. | 溶液一定是无色透明的液体 | |
| B. | 溶液稀释前后,溶质质量不变 | |
| C. | 溶液都能导电 | |
| D. | 在其它条件不变时,氮气的溶解度随压强的升高而减小 |
4.下列关于实验现象的描述正确的是( )
| A. | 铁丝在氧气中燃烧生成四氧化三铁 | |
| B. | 二氧化碳通入紫色石蕊溶液中,溶液变为蓝色 | |
| C. | 电解水实验中,正极端与负极端产生的气体体积比约为1:2 | |
| D. | 氢气在空气中燃烧产生黄色火焰 |
1.小明同学i所学部分化学知识归纳如下,其中有错误的是( )
| A. | 物质用途:稀有气体-焊接金属的保护气 | |
| B. | 安全常识:煤气泄漏-关闭气阀、严禁烟火 | |
| C. | 元素与人体健康:缺钙-骨质疏松,易得佝偻病 | |
| D. | 生活经验:除去热水瓶中的水垢-用食盐水检验 |