题目内容
19.分别把4g硫粉放在给定质量的氧气中燃烧,有关实验数据如表所示.请回答下列问题.| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 5 |
| SO2质量(g) | 6 |
(2)请你通过计算求出第二次和第三次实验生成的二氧化硫的质量.
(3)上述三次实验中,第一、二、三次符合质量守恒定律.
分析 本题设计本意好像不能去根据方程式计算,但是根据4g硫粉和3g氧气得到6g却不能判断硫单质和氧气之间的关系,所以还是要根据化学方程式计算.而不能简单猜测为3g硫粉和3g氧气反应生成6g二氧化硫.
解答 解:(1)硫和氧气反应生成二氧化硫,方程式和质量关系如下
S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
32 32 64
1 1 2
也就是在反应中参加反应的硫、氧气、生成的二氧化硫的质量比为1:1:2
在第一次实验中硫粉有剩余
第二次实验中,硫粉和氧气的质量均为4g,根据“参加反应的硫、氧气、生成的二氧化硫的质量比为1:1:2”,可知此时硫粉和氧气恰好完全反应生成8g的二氧化硫.
第三次加入的氧气为5g,而硫只有4g,所以氧气有剩余,参加反应的氧气为4g,生成的二氧化硫为8g
以上三次实验均符合质量守恒定律,质量守恒定律,强调参加反应的物质的质量总和等于生成物的质量总和,不是说加多少就算多少,而是实际反应和实际生成的.
答:(1)第一次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是 1:1:2;
(2)请你通过计算求出第二次和第三次实验生成的二氧化硫的质量均为8g.
(3)上述三次实验中,第 一、二、三次符合质量守恒定律.
点评 质量守恒定律适合所有的化学反应,针对的是实际参加反应的物质和实际生成的物质,而不是提供多少都理解为反应物,也就是说只有反应掉的那部分才叫反应物.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
9.日常生活中的下列变化,属于物理变化的是( )
| A. | 木柴燃烧 | B. | 冰雪融化 | C. | 光合作用 | D. | 食物变质 |
10.为了探究蜡烛燃烧的现象,点燃蜡烛灯后,取一根火柴梗平放在蜡烛火焰中,约1s~2s后取出,请你继续帮忙完成下列实验报告:
| 实验步骤 | 实验现象 | 结 论 |
| 点燃蜡烛,将一根火柴横在火焰上方; | 火柴梗两端最先烧焦. | 酒精灯的火焰分为外焰、内焰、焰心.外焰的温度最高. |
| 将一只干冷的烧杯罩在火焰上方; | 烧杯内壁出现水雾. | 说明蜡烛燃烧生成了水 |
| 将一只内壁附有澄清石灰水的烧杯罩在火焰上方. | 石灰水变变浑浊. | 说明蜡烛燃烧还生成二氧化碳 |
7.如图所示变化中,属于化学变化的是( )
| A. |  冰雪融化 | B. |  干冰升华 | C. |  蜡烛燃烧 | D. |  菠萝榨汁 |
7.2016年环境日主题为“改善环境质量推动绿色发展”,旨在引导社会各界着力践行人与自然和谐共生和绿色发展理念,从身边小事做起,共同履行环保责任,改善环境质量,共建美丽家园.下列做法符合这一主题的是( )
| A. | 大量焚烧秸秆,增加土壤肥力 | B. | 大量使用化肥、农药,以增产增收 | ||
| C. | 减少私家车使用,尽量步行 | D. | 使用一次性筷子,以保证人体健康 |
4.按如图所示操作完成实验,对实验结果分析正确的是( )
| A. | 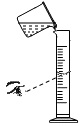 量取10ml液体:实际所得液体体积小于10ml | |
| B. |  检查气密性:导管口有气泡,则装置漏气 检查气密性:导管口有气泡,则装置漏气 | |
| C. |  测定空气中O2 的含量:瓶内水面上升体积大于瓶内空气体积的$\frac{1}{5}$ | |
| D. |  称取25g物质:实际称得固体质量大于25g |