题目内容
1. 眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图
眼镜是人们常用的护眼工具,如图是一款变色眼镜的示意图(1)所标元件中,由金属单质制成的是铜螺丝.
(2)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜.在强光照射下,溴化银分解成溴和银,玻璃颜色变深,此反应类型属于分解反应;当光线变暗时,溴和银在氧化铜作用下,重新生成溴化银,玻璃颜色变浅;氧化铜在该反应中起催化作用.
分析 (1)根据材料的分类知识进行分析;
(2)根据基本反应类型的判断方法以及溴单质和银在氧化铜作用下,能够重新生成溴化银,说明氧化铜在反应中起到催化剂的作用.
解答 解:(1)铜螺丝属于金属单质,故填:铜螺丝;
(2)强光照射下,溴化银分解成溴单质和银的化学方程式为:2AgBr$\frac{\underline{\;强光\;}}{\;}$2Ag+Br2;此反应是“一变多”属于分解反应;当光线变暗时,溴单质和银在氧化铜作用下,又重新生成溴化银,玻璃颜色变浅,氧化铜在该反应中本身没有变化,起催化作用.故填:分解;催化.
点评 本题考查物质的分类,基本反应类型的判断,催化剂的作用等,难度不大,基础性较强.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
1.资源是指一个国家或一定地区内拥有的物力、人力、财力等各种物质要素的总称,在对下列资源的利用过程中,发生了化学变化的是( )
| A. | 海水晒盐 | B. | 木头制作家具 | C. | 水力发电 | D. | 冶炼铜矿 |
12.下列实验方案设计不合理的是( )
| 选项 | 实验内容 | 操作或所用试剂 |
| A | 鉴别铁粉和木炭粉 | 观察颜色 |
| B | 除去氯化钾溶液中的硫酸钾 | 加入适量氯化钡溶液,过滤 |
| C | 鉴别羊毛和合成纤维 | 取样、灼烧,闻气味 |
| D | 鉴别氮气和氧气 | 燃着的木条 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
9.已知氯化钠、碳酸钠在不同温度时的溶解度如表.下列说法正确的是( )
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 10 | 18 | 36.5 | 50 | |
| A. | NaCl的溶解度大于Na2CO3的溶解度 | |
| B. | NaCl和Na2CO3都是易溶物质 | |
| C. | 20℃时,100gNaCl饱和溶液中含NaCl 36g | |
| D. | 若NaCl中混有少量Na2CO3,可用降温结晶的方法提纯 |
6.某科技兴趣小组同学为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如表:
(1)该黄铜样品中铜的质量是67.5克.
(2)第2次测得剩余固体质量为74g,其成分为C.
A.铜B.锌C.铜和锌
(3)实验所用的稀硫酸的质量分数多大?
(4)第3次加入稀硫酸充分反应后所得溶液的溶质是硫酸锌和硫酸;.
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
(2)第2次测得剩余固体质量为74g,其成分为C.
A.铜B.锌C.铜和锌
(3)实验所用的稀硫酸的质量分数多大?
(4)第3次加入稀硫酸充分反应后所得溶液的溶质是硫酸锌和硫酸;.
13.梧州市某中学化学兴趣小组的同学发现,熟鸡蛋在常温下放置一、两天后就会变臭了.富有营养而鲜美的鸡蛋,怎么会散发出臭味呢?同学们旋即对此进行了研究.
【提出问题】这种散发出刺激性臭味的无色气体是什么?它有怎样的性质?
【猜想假设】大家按照查阅到的鸡蛋中主要含有的元素是 C、H、O、N、S 的信息,及相应元素的化合价,列出了气体的可能存在形式分别有以下几组:
甲组-含碳化合物:CH4、CO、CO2
乙组-含氮化合物:NH3、NO、NO2
丙组-含硫化合物:SO2、SO3
虽然列出了上述可能,但大家都一致提议排除甲组的可能性,大家提出的理由是:甲组气体均为无色无味气体.
【查阅资料】
根据所查阅的资料,大家进一步排除了 NO、NO2,理由是NO2是红棕色气体,而NO在空气中会变成NO2;也排除了 SO3的可能,理由是常温下SO3不是气体.
【实验验证】毫无头绪的同学们向老师请教,老师笑而不语,拿出了两集气瓶的气体 M,告诉大家这就是该刺激性臭味气体的主要成分,具有可燃性,至于还有什么性质,让大家在注意防护和试验安全的条件下进行探究.
(1)小吴同学用针筒抽取了部分气体 M,注入盛有石蕊试液的试管中,结果没有看到溶液变的现象,证明该气体不是 NH3;
(2)小周同学设法点燃了气体 M,并拿一个干冷的小烧杯罩在火焰的上方,看到烧杯内壁有小水珠出现,说明了 M 气体中含有H 元素;燃烧后的气体带有刺激性,并能使另一个内壁沾有 KMnO4溶液的小烧杯,出现红色褪去的现象,说明 M 气体中还含有S 元素.
(3)为了进一步探究 M 气体的组成,小施将 3.4g 的 M 气体完全燃烧后,设法将燃烧后所得气体,全部通入如图装置进行中.(注:碱石灰为固体 NaOH 和 CaO 的混合物)
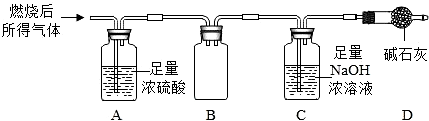
经充分吸收后称重,发现 A 装置增重 1.8g,C 装置增重 6.4g.通过计算可知,除了上述小周确定的两种元素外,M 气体中不含(填“含”或“不含”)其他元素;并确定了 M 的化学式为H2S.而上图中 B 装置的作用是防倒吸作用;D 装置的作用是防空气中的二氧化碳和水蒸气进入测量体系.
【提出问题】这种散发出刺激性臭味的无色气体是什么?它有怎样的性质?
【猜想假设】大家按照查阅到的鸡蛋中主要含有的元素是 C、H、O、N、S 的信息,及相应元素的化合价,列出了气体的可能存在形式分别有以下几组:
甲组-含碳化合物:CH4、CO、CO2
乙组-含氮化合物:NH3、NO、NO2
丙组-含硫化合物:SO2、SO3
虽然列出了上述可能,但大家都一致提议排除甲组的可能性,大家提出的理由是:甲组气体均为无色无味气体.
【查阅资料】
| 物质 | NH3 | NO | NO2 | SO2 | SO3 |
| 一些特性 | 碱性 | 在空气中会迅速变成 NO2 | 红棕色 | 酸性,有刺激性气味,能使 KMnO4溶液褪色 | 沸点 44.8℃ |
【实验验证】毫无头绪的同学们向老师请教,老师笑而不语,拿出了两集气瓶的气体 M,告诉大家这就是该刺激性臭味气体的主要成分,具有可燃性,至于还有什么性质,让大家在注意防护和试验安全的条件下进行探究.
(1)小吴同学用针筒抽取了部分气体 M,注入盛有石蕊试液的试管中,结果没有看到溶液变的现象,证明该气体不是 NH3;
(2)小周同学设法点燃了气体 M,并拿一个干冷的小烧杯罩在火焰的上方,看到烧杯内壁有小水珠出现,说明了 M 气体中含有H 元素;燃烧后的气体带有刺激性,并能使另一个内壁沾有 KMnO4溶液的小烧杯,出现红色褪去的现象,说明 M 气体中还含有S 元素.
(3)为了进一步探究 M 气体的组成,小施将 3.4g 的 M 气体完全燃烧后,设法将燃烧后所得气体,全部通入如图装置进行中.(注:碱石灰为固体 NaOH 和 CaO 的混合物)

经充分吸收后称重,发现 A 装置增重 1.8g,C 装置增重 6.4g.通过计算可知,除了上述小周确定的两种元素外,M 气体中不含(填“含”或“不含”)其他元素;并确定了 M 的化学式为H2S.而上图中 B 装置的作用是防倒吸作用;D 装置的作用是防空气中的二氧化碳和水蒸气进入测量体系.
 等质量的铁粉和锌粉,加入足量等浓度的稀硫酸中,不考虑浓度和温度等对反应速度的影响,请你在图中画出产生氢气的质量与时间关系的大致图象,并说明理由.
等质量的铁粉和锌粉,加入足量等浓度的稀硫酸中,不考虑浓度和温度等对反应速度的影响,请你在图中画出产生氢气的质量与时间关系的大致图象,并说明理由.