题目内容
(2011?东城区二模)甲物质是一种重要的有机化工原料.一定质量的甲和48g乙按如图所示充分反应,当乙完全反应时,可生成44g丙和36g丁,则甲中所含各元素的质量比为( )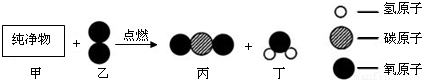
【答案】分析:由已知“将一定质量的甲与48g乙按下图所示充分反应,当乙反应完全时,生成44克丙和36克丁”,根据质量守恒定律,则可求甲参加反应的质量;结合模型图可推测C为二氧化碳,丁为水,可以求出二氧化碳中的碳元素的质量,水中氢元素的质量,即A中各元素的质量比;
解答:解:由已知“将一定质量的甲与48g乙按下图所示充分反应,当乙反应完全时,生成44克丙和36克丁”,根据质量守恒定律,则可求甲参加反应的质量为:44+36-48=32克;结合模型图可推测丙为二氧化碳,丁为水,则“44g丙和36g丁”二氧化碳中的碳元素的质量为44克×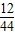 ×100%=12克,水中氢元素的质量为36克×
×100%=12克,水中氢元素的质量为36克×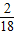 ×100%=4克;因为碳元素、氢元素都来自甲,故甲中各元素的质量比m(C):m(H)=12:4;生成物中的氧元素的质量是44+36-12-4=64g,而反应物中氧气提供的氧元素的质量是48g,所以甲中含有的氧元素的16g,所以碳氢氧的质量比是3:1:4.
×100%=4克;因为碳元素、氢元素都来自甲,故甲中各元素的质量比m(C):m(H)=12:4;生成物中的氧元素的质量是44+36-12-4=64g,而反应物中氧气提供的氧元素的质量是48g,所以甲中含有的氧元素的16g,所以碳氢氧的质量比是3:1:4.
故选D
点评:了解微粒观点及模型图的应用;掌握原子的有关数量计算;依据质量守恒定律进行元素质量比的计算是解题的关键.
解答:解:由已知“将一定质量的甲与48g乙按下图所示充分反应,当乙反应完全时,生成44克丙和36克丁”,根据质量守恒定律,则可求甲参加反应的质量为:44+36-48=32克;结合模型图可推测丙为二氧化碳,丁为水,则“44g丙和36g丁”二氧化碳中的碳元素的质量为44克×
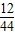 ×100%=12克,水中氢元素的质量为36克×
×100%=12克,水中氢元素的质量为36克×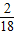 ×100%=4克;因为碳元素、氢元素都来自甲,故甲中各元素的质量比m(C):m(H)=12:4;生成物中的氧元素的质量是44+36-12-4=64g,而反应物中氧气提供的氧元素的质量是48g,所以甲中含有的氧元素的16g,所以碳氢氧的质量比是3:1:4.
×100%=4克;因为碳元素、氢元素都来自甲,故甲中各元素的质量比m(C):m(H)=12:4;生成物中的氧元素的质量是44+36-12-4=64g,而反应物中氧气提供的氧元素的质量是48g,所以甲中含有的氧元素的16g,所以碳氢氧的质量比是3:1:4.故选D
点评:了解微粒观点及模型图的应用;掌握原子的有关数量计算;依据质量守恒定律进行元素质量比的计算是解题的关键.

练习册系列答案
相关题目
(2011?东城区二模)为探究四瓶未知无色溶液的成分,甲、乙、丙三组同学分别设计了如下实验.已知四种溶液分别是Na2CO3,NaOH、Ca(OH)2和稀盐酸中的一种.
实验过程
甲组实验方案:将四瓶溶液标号分别为1,2,3,4,只利用紫色石蕊溶液进行实验.
乙组实验方案:不用其他试剂进行实验.
实验分析
经过交流后,发现实验结论______(填序号)是不正确的;若该结论作正确,对应的实验现象应是______.
丙组实验方案:将四种溶液编号为1,2,3,4,不用其他试剂进行实验.
实验过程
甲组实验方案:将四瓶溶液标号分别为1,2,3,4,只利用紫色石蕊溶液进行实验.
| 实验步骤和操作 | 实验现象和结论 |
(1)如图所示: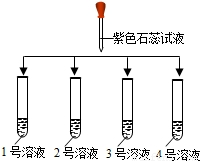 | ①2号溶液由无色变为红色, 则2号溶液是______ ②另三支试管中溶液均由无色变蓝色 |
(2)另取1、3、4号溶液,分别滴加2号溶液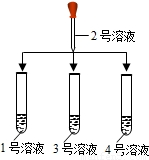 | ①3号溶液中有气泡放出, 则3号溶液是______ ②另外二支试管中溶液无明显变化 |
| (3)另取1,4号溶液,分别滴加______ | ①1号溶液中有白色沉淀析出, 则反应的化学方程式为______ ②另一支试管中溶液中无明显变化 |
| 实验操作 | 实验现象 | 实验结论 |
任取三种溶液于三支试管中,分别滴加第四种溶液 | ①一支试管中有气泡放出 其余二支试管中溶液无明显变化 | ①第四种溶液为稀盐酸 |
| ②一支试管中有白色沉淀析出, 其余二支试管中溶液无明显变化 | ②第四种为Na2CO3溶液 | |
| ③三支试管中溶液均无明显变化 | ③第四种为NaOH溶液 |
经过交流后,发现实验结论______(填序号)是不正确的;若该结论作正确,对应的实验现象应是______.
丙组实验方案:将四种溶液编号为1,2,3,4,不用其他试剂进行实验.
| 实验操作 | 实验现象 | 实验结论 |
如图所示: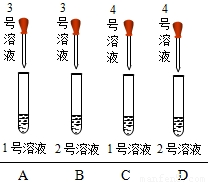 | ①A,B,C均无明显变化 ②D中有沉淀析出 | 标号为1,2,3,4的溶液依次为(用化学式表示): ______或______ |
(2011?东城区二模)钢铁是使用最多的金属材料.
(1)下图为实验室炼铁的装置图,A中反应的化学方程式是;将反应后的气体通过装置B和C,收集较纯净的CO并循环使用,B中应盛放的试剂是浓溶液.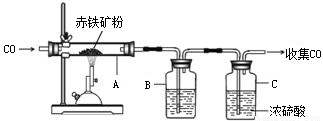
(2)工业上可用酸清洗锈蚀的金属.将生锈的铁片和生锈的铜片[铜锈的成分是Cu2(OH)2CO3]同时放入一定量盐酸中,可能发生的化学反应有:
①铜锈溶解:Cu2(OH)2CO3+4HCl=2CuCl2+3X+CO2↑,则X的化学式为;
②铁锈溶解:化学方程式为;
③有金属单质生成:化学方程式为.
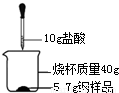
(3)某化学小组欲测定一种钢样品中铁的含量,实验操作如图所示,实验结果记录如下表:
①经计算,这种钢样品中铁的含量是% (精确到0.1%).
②有同学提出,灼烧可使钢中的碳转化为二氧化碳,钢样品质量会减轻.但是他们将一定量的钢样品灼烧后,发现质量反而增加了,其原因是 .
(1)下图为实验室炼铁的装置图,A中反应的化学方程式是;将反应后的气体通过装置B和C,收集较纯净的CO并循环使用,B中应盛放的试剂是浓溶液.

(2)工业上可用酸清洗锈蚀的金属.将生锈的铁片和生锈的铜片[铜锈的成分是Cu2(OH)2CO3]同时放入一定量盐酸中,可能发生的化学反应有:
①铜锈溶解:Cu2(OH)2CO3+4HCl=2CuCl2+3X+CO2↑,则X的化学式为;
②铁锈溶解:化学方程式为;
③有金属单质生成:化学方程式为.
(3)某化学小组欲测定一种钢样品中铁的含量,实验操作如图所示,实验结果记录如下表:
| 反应时间 | t | t1 | t2 | t3 |
| 烧杯和药品质量/g | 55.7 | 55.6 | 55.5 | 55.5 |
②有同学提出,灼烧可使钢中的碳转化为二氧化碳,钢样品质量会减轻.但是他们将一定量的钢样品灼烧后,发现质量反而增加了,其原因是 .