题目内容
13.在工业上用纯碱和石灰石为原料制备烧碱,主要流程如图所示: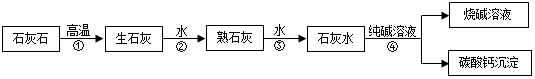
(1)在①-④四个过程中,发生了复分解反应的是④(填序号).
(2)欲检验烧碱溶液中含有少量Na2CO3,请从酚酞试液、稀盐酸、石灰水中选用一种合适的试剂进行实验,简述具体检验方法取少量NaOH溶液样品于试管中,加入适量稀盐酸,若产生气泡,说明NaOH溶液发生了变质.
(3)在室温下,将53g质量分数为10%的Na2CO3溶液与3000g澄清石灰水充分混合,恰好完全反应.所得纯NaOH的质量是多少?
分析 (1)根据流程图碳酸钙在高温下生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠分析反应的类型;
(2)根据碳酸根离子的验证分析;
(3)利用氢氧化钙与碳酸钠反应的化学方程式中碳酸钠的质量计算生成沉淀的质量,然后根据质量守恒定律计算氢氧化钠溶液的质量.
解答 解:(1)碳酸钙在高温下生成氧化钙和二氧化碳,属于分解反应;氧化钙和水反应生成氢氧化钙,属于化合反应;氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,属于复分解反应;
(2)检验烧碱溶液中含有少量Na2CO3,要先验证碳酸根离子,可取少量NaOH溶液样品于试管中,加入适量稀盐酸,若产生气泡,说明NaOH溶液发生了变质;(或取少量NaOH溶液样品于试管中,向试管中加入适量的Ca(OH)2溶液,若产生白色沉淀,说明NaOH溶液确实发生了变质);
(3)设生成氢氧化钠的质量为x
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
106 80
53g×10% x
$\frac{106}{53g×10%}=\frac{80}{x}$
x=4g
答:所得NaOH的质量是4g.
故答案为:(1)④;(2)取少量NaOH溶液样品于试管中,加入适量稀盐酸,若产生气泡,说明NaOH溶液发生了变质;(或取少量NaOH溶液样品于试管中,向试管中加入适量的Ca(OH)2溶液,若产生白色沉淀,说明NaOH溶液确实发生了变质)
(3)4g.
点评 本题考查了根据反应的流程完成反应原理及基本反应类型的判断、碳酸根离子的检验及相关的计算,根据碳酸钙离子的检验方法及化学方程式的计算即可完成.

 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案| 选 项 | 操作或现象 | 微粒的特性 |
| A | 给自行车胎打气 | 分子间有间隙 |
| B | 校园内远远闻到桂花的香味 | 分子在不断运动 |
| C | 100mL酒精和100mL水混合在一起,体积小于200mL | 分子是很微小的 |
| D | 电解水可以得到氢气和氧气 | 分子是可以再分的 |
| A. | A | B. | B | C. | C | D. | D |
| 现象或事实 | 解释 | |
| A | 物体热胀冷缩 | 分子体积随温度改变而改变 |
| B | 山村梅开处处香 | 分子总在不断地运动 |
| C | O2可供人呼吸,H2可以做燃料 | 构成物质的分子不同,则性质不同,用途不同 |
| D | 酸都有相似的化学性质 | 酸溶液中都含有H+ |
| A. | A | B. | B | C. | C | D. | D |
 水是生命之源.请回答下列问题:
水是生命之源.请回答下列问题:
