题目内容
1.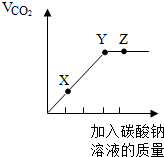 如图所示是化学兴趣小组研究复分解反应的实验中,将Na2CO3溶液逐滴加入盐酸中,产生二氧化碳的体积随滴入Na2CO3溶液质量变化的曲线图.下列说法中正确的是( )
如图所示是化学兴趣小组研究复分解反应的实验中,将Na2CO3溶液逐滴加入盐酸中,产生二氧化碳的体积随滴入Na2CO3溶液质量变化的曲线图.下列说法中正确的是( )| A. | 若向图中X点的溶液中滴加石蕊试液,溶液会变为红色 | |
| B. | 图中Y点溶液中的碳酸钠和盐酸恰好完全反应 | |
| C. | 图中Z点的溶液中不含溶质NaCl | |
| D. | 图中Y→Z的过程中,溶液中氯化钠的质量分数没有变化 |
分析 根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,依据图象中二氧化碳的变化趋势进行分析.
解答 解:A、通过分析可知,将碳酸钠逐滴加入盐酸中,所以X点应是盐酸过量,滴加石蕊溶液应变红,故A正确;
B、图中Y点二氧化碳的体积达到了最大值,所以Y点溶液中的碳酸钠和盐酸恰好完全反应,故B正确;
C、图中Z点表示盐酸过量,所以溶液中含有的溶质是NaCl、HCl,故C错误;
D、图中Y→Z的过程中,氯化钠的质量不再改变,溶液的质量逐渐增大,所以溶液中氯化钠的质量分数逐渐减小,故D错误.
故选:AB.
点评 本题主要考查了分析图中数据的能力,注意反应原理和图象转折点的正确理解.

练习册系列答案
相关题目
2. NaCl和KNO3两种物质的溶解度曲线如图所示.下列说法正确的是( )
NaCl和KNO3两种物质的溶解度曲线如图所示.下列说法正确的是( )
 NaCl和KNO3两种物质的溶解度曲线如图所示.下列说法正确的是( )
NaCl和KNO3两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃时,NaCl的不饱和溶液降温一定会变成饱和溶液 | |
| B. | t2℃时,KNO3溶液降温后一定有晶体析出 | |
| C. | t1℃时,NaCl和KNO3的溶液各100 g,其溶质的质量一定相等 | |
| D. | t2℃时,KNO3饱和溶液中溶质质量分数一定大于NaCl溶液中溶质质量分数 |
9.下列实验中的替代品使用正确的是( )
| A. | 实验室制氢气时,用铁片替代锌片 | |
| B. | 实验室制二氧化碳时,用石灰石替代大理石 | |
| C. | 采用分解过氧化氢的方法制氧气时,用KMnO4替代MnO2 | |
| D. | 用浓碳酸钠溶液和饱和石灰水制取氢氧化钠,用氢氧化钾溶液替代石灰水 |
16.二氧化碳与二氧化硫同为非金属氧化物,某兴趣小组用类比法进行如下探究: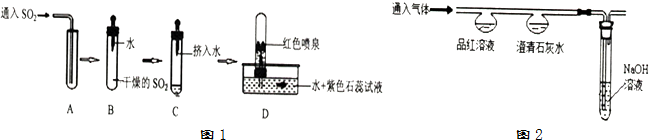
探究一:SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是AB(填序号,可多选).
A、反应物的状态 B、反应条件 C、气体密度 D、气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验
通过上述实验,可推测SO2气体的性质有:①二氧化硫密度比空气大;②二氧化硫能溶于水.
探究二:CO2和SO2性质的比较
兴趣小组设计并进行如图2的实验,探究比较CO2和SO2的化学性质.
(3)由实验可知:
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式Ca(OH)2+SO2═CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去的是二氧化硫,无明显变化的是二氧化碳.
③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色
②二氧化碳与碘水反应的化学方程式为:SO2+I2+2H2O═H2SO4+2HI(SO2、I2的相对分子质量分别为64.254)
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
(4)测定步骤:
Ⅰ.检查装置的气密性
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)由实验可知:
①当溶液由蓝色变成无色时反应恰好完全
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填如表中所列举的等级).

探究一:SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是AB(填序号,可多选).
A、反应物的状态 B、反应条件 C、气体密度 D、气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验
通过上述实验,可推测SO2气体的性质有:①二氧化硫密度比空气大;②二氧化硫能溶于水.
探究二:CO2和SO2性质的比较
兴趣小组设计并进行如图2的实验,探究比较CO2和SO2的化学性质.
| 实验Ⅰ | 实验Ⅱ | |
| 通入CO2 | 通入SO2 | |
| 品红溶液 | 无明显变化 | 红色褪为无色 |
| 澄清石灰水 | 白色浑浊 | 白色浑浊 |
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式Ca(OH)2+SO2═CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去的是二氧化硫,无明显变化的是二氧化碳.
③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色
②二氧化碳与碘水反应的化学方程式为:SO2+I2+2H2O═H2SO4+2HI(SO2、I2的相对分子质量分别为64.254)
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
| SO2最高浓度限值(单位mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
Ⅰ.检查装置的气密性
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)由实验可知:
①当溶液由蓝色变成无色时反应恰好完全
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填如表中所列举的等级).
6.小林发现妈妈在面粉中加入一种白色粉末,做出的馒头疏松多孔.他很感兴趣,想探究这种白色粉末的成分.通过对市场上相关产品进行调查,她发现了如下表所示的三种商品,猜想妈妈使用的白色粉末是如表三种商品中的一种.
(1)纯碱的化学式是Na2CO3,它的水溶液的PH>7.图表中的三种商品都能在使用过程中产生一种气体,使做成的馒头疏松多孔,这种气体是CO2.
(2)方案一:据获得的信息,小林设计实验方案一,在实验室探究这种白色粉末的成分.
(3)老师提示小林②③得出的结论有不足之处,原因是碳酸钠和碳酸氢钠都能与盐酸反应放出使澄清石灰水变浑浊的气体,无法判定样品是哪种.经过查阅资料和老师的帮助小林改进实验方案,确认白色粉末的成分.
方案二:样品与盐酸反应生成气体的比较
已知查阅资料碳酸氢钠4.2g和碳酸钠5.3g完全反应生成的气体体积都为Vml,如图所示.图I是反应装置,图Ⅱ装置能测量出反应生成气体的体积.
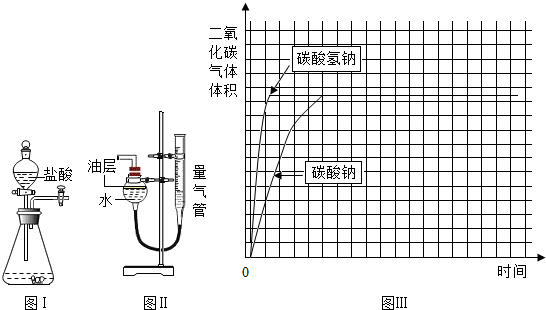
(1)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(2)数据与分析:根据图Ⅲ曲线,可得生成相同体积的二氧化碳气体,碳酸氢钠比碳酸钠的速度快(快或慢)
(3)小林参考已知的实验方案在图I锥形瓶中加入了5.3g的白色粉末(杂质等因素均忽略),分液漏斗加入已知相同浓度的盐酸(足量).产生气体的体积大于(大于、小于、等于)Vml,证明猜想②是正确的.
| 猜想 | ① | ② | ③ |
| 商品 | 食用纯碱 | 食用小苏打 | 快速发酵粉 |
| 成分 | 碳酸钠 | 碳酸氢钠 | 碳酸氢钠、有机酸 |
| 用法 | 面粉加水揉和成面团,发酵后产生酸味,加入适量纯碱,反复揉和,加热即可制成松软的馒头. | 面粉无需发酵,直接加入适量小苏打,加水调和,放入烤箱加热即可制成疏松多孔的糕点. | 面粉与发酵粉按比例拌匀,放入适量温水揉和,放置一段时间,即可蒸、烘、烤制成疏松多孔的各种食品. |
(2)方案一:据获得的信息,小林设计实验方案一,在实验室探究这种白色粉末的成分.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白色粉末于试管中,加入适量温蒸馏水揉和,放置一段时间. | 固体溶解,无其他明显现象. | 猜想3是错误的 |
| ②取少量白色粉末于试管中,加入适量蒸馏水,滴加稀盐酸; ③将产生的气体通入澄清的石灰水. | 有无色气泡产生; 澄清的石灰水变浑浊. | 猜想①是正确的实验操作有关的化学方程式2HCl+Na2CO3=2NaCl+H2O+CO2↑ 2HCl+Na2CO3=2NaCl+H2O+CO2↑. |
方案二:样品与盐酸反应生成气体的比较
已知查阅资料碳酸氢钠4.2g和碳酸钠5.3g完全反应生成的气体体积都为Vml,如图所示.图I是反应装置,图Ⅱ装置能测量出反应生成气体的体积.

(1)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(2)数据与分析:根据图Ⅲ曲线,可得生成相同体积的二氧化碳气体,碳酸氢钠比碳酸钠的速度快(快或慢)
(3)小林参考已知的实验方案在图I锥形瓶中加入了5.3g的白色粉末(杂质等因素均忽略),分液漏斗加入已知相同浓度的盐酸(足量).产生气体的体积大于(大于、小于、等于)Vml,证明猜想②是正确的.
13.如表归纳内容全部正确的组别是( )
| A.解释说明 | B.化学与生活 |
| ①稀有气体作保护气--化学性质稳定 ②O2、CO2化学性质不同--分子构成不同 ③众人拾柴火焰高--可燃物越多,燃烧越旺 | ①蛋白质、油脂、糖类都能为人体提供能量 ②人体所需维生素量不多,但不能缺少 ③玻璃钢、铝合金都是金属材料 |
| C.化学用语中数字的含义 | D.方程式表示所述内容 |
| ①H2O:一个水分子含有两个氢原子 ②$\stackrel{+2}{Ca}$:一个钙离子带有两个单位正电荷 ③$\stackrel{-2}{S}$:硫元素的化合价为负二价 | ①酸雨形成CO2+H2O═H2CO3 ②治疗胃酸过多Al(OH)3 +3HCl═AlCl3+3H2O ③铝制品耐腐的原因:4Al+3O2═2Al2O3 |
| A. | A | B. | B | C. | C | D. | D |
10.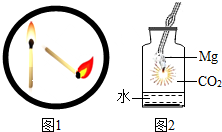 下列关于燃烧与灭火的说法正确的是( )
下列关于燃烧与灭火的说法正确的是( )
 下列关于燃烧与灭火的说法正确的是( )
下列关于燃烧与灭火的说法正确的是( )| A. | 将大块煤粉碎后再燃烧,其目的是延长煤燃烧的时间 | |
| B. | 由图1 可知,火柴头斜向下降低了火柴梗的着火点 | |
| C. | 由图2 可知,金属镁引起的火灾不能用CO2 灭火 | |
| D. | 蜡烛用扇子一扇即灭,是因为扇走了蜡烛周围的空气 |
11.化学在能源利用、环境保护等方面起着重要的作用,下列有关做法错误的是( )
| A. | 变废为宝,将地沟油转化为航空燃油 | |
| B. | 为治理雾霾,减少使用化石燃料 | |
| C. | 城市道路使用太阳能景观灯,节能又环保 | |
| D. | 用二氧化碳和水等合成新型燃油,不利于减缓温室效应 |