题目内容
“神州七号”飞船的成功发射是我国航天事业的又一里程碑.“神州七号”太空舱利改变了“神舟”六号利用过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气的原理,而是采用NiFe2O4将航天员呼出的CO2转化为O2,而NiFe2O4的质量和化学性质都不变化,从而减少携带物品的质量.
(1)在该过程中NiFe2O4是 .若NiFe2O4中Fe的化合价为+3价,则Ni的化合价为 .
(2)过氧化钠和二氧化碳反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2↑.为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图所示的实验.
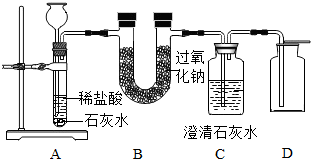
A装置中所发生反应的化学方程式为 ;实验前,把A、B、C、D中的玻璃管相连时,都是通过胶皮管连接,为了能顺利地连接,你的方法是 ;检查A装置的气密性的方法是:将A装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到 现象,即可证明装置不漏气.
(3)表明二氧化碳没有被过氧化钠完全吸收的现象是 .
(4)用向上排空气法收集氧气,并用带火星的木条放在集气瓶口检验氧气是否收集满,这是利用了氧气的哪些性质?
(5)常温下水也能与Na2O2反应,生成氧气和氢氧化钠,写出该反应的化学方程式.若要检验干燥的二氧化碳能否与过氧化钠反应生成氧气,以上实验装置应如何改进?
(6)某潜水艇上有4人,如果每人每小时消耗的氧气在某温度和压强条件下体积为50L,则该潜水艇中每天需要过氧化钠多少千克?(已知:在上述温度和压强条件下氧气的密度为1.5g/L)
(1)在该过程中NiFe2O4是
(2)过氧化钠和二氧化碳反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2↑.为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图所示的实验.

A装置中所发生反应的化学方程式为
(3)表明二氧化碳没有被过氧化钠完全吸收的现象是
(4)用向上排空气法收集氧气,并用带火星的木条放在集气瓶口检验氧气是否收集满,这是利用了氧气的哪些性质?
(5)常温下水也能与Na2O2反应,生成氧气和氢氧化钠,写出该反应的化学方程式.若要检验干燥的二氧化碳能否与过氧化钠反应生成氧气,以上实验装置应如何改进?
(6)某潜水艇上有4人,如果每人每小时消耗的氧气在某温度和压强条件下体积为50L,则该潜水艇中每天需要过氧化钠多少千克?(已知:在上述温度和压强条件下氧气的密度为1.5g/L)
考点:催化剂的特点与催化作用,实验探究物质的组成成分以及含量,检查装置的气密性,常见气体的检验与除杂方法,氧气的检验和验满,二氧化碳的化学性质,有关元素化合价的计算,根据化学反应方程式的计算
专题:化学与新科技
分析:(1)据催化剂的概念,化合物中各元素化合价代数和为零得出.
(2)书写碳酸钙与盐酸反应的化学方程式即可;据导管的连接;向试管中加入水如果装置不漏气,容器内的气压会不断变大.
(3)C中的澄清石灰水可以证明有无二氧化碳存在;
(4)收集气体的方法是利用的气体的物理性质,验满是利用的氧气的助燃性
(5)方程式可利用信息书写;二氧化碳通入B装置前要进行干燥处理
(6)根据化学方程式的计算解决,先要对消耗的氧气进行体积与质量的转化,再利用2Na2O2+2CO2═2Na2CO3+O2求过氧化钠的质量
(2)书写碳酸钙与盐酸反应的化学方程式即可;据导管的连接;向试管中加入水如果装置不漏气,容器内的气压会不断变大.
(3)C中的澄清石灰水可以证明有无二氧化碳存在;
(4)收集气体的方法是利用的气体的物理性质,验满是利用的氧气的助燃性
(5)方程式可利用信息书写;二氧化碳通入B装置前要进行干燥处理
(6)根据化学方程式的计算解决,先要对消耗的氧气进行体积与质量的转化,再利用2Na2O2+2CO2═2Na2CO3+O2求过氧化钠的质量
解答:解:(1)反应前后NiFe2O4的质量和化学性质都不变化其应为催化剂;据化合物NiFe2O42中各元素化合价代数和为零得出Ni的化合价为+2价
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;据导管的连接先把玻璃管的一端润湿,再旋转插入; 漏斗颈中形成一段稳定的水柱(或液面不再下降)
(3)据二氧化碳能澄清石灰水变浑浊故应填C装置处的澄清石灰水变浑浊.
(4)氧气的密度比空气大,氧气能支持燃烧.
(5)2Na2O2+2H2O═4NaOH+O2↑;在A、B装置之间增加气体干燥装置
(6)解:50L氧气的质量为:50 L×1.5g/L=75g
该潜水艇中每天消耗氧气的质量为:4×24×75g=7200g即7.2kg(1分)
设该潜水艇中每天需要过氧化钠的质量为x.
2Na2O2+2CO2=2Na2CO3+O2↑
156 32
x 7.2kg
156/32=x/7.2kg
x=35.1kg
答:该潜水艇中每天需要过氧化钠35.1kg.
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑;据导管的连接先把玻璃管的一端润湿,再旋转插入; 漏斗颈中形成一段稳定的水柱(或液面不再下降)
(3)据二氧化碳能澄清石灰水变浑浊故应填C装置处的澄清石灰水变浑浊.
(4)氧气的密度比空气大,氧气能支持燃烧.
(5)2Na2O2+2H2O═4NaOH+O2↑;在A、B装置之间增加气体干燥装置
(6)解:50L氧气的质量为:50 L×1.5g/L=75g
该潜水艇中每天消耗氧气的质量为:4×24×75g=7200g即7.2kg(1分)
设该潜水艇中每天需要过氧化钠的质量为x.
2Na2O2+2CO2=2Na2CO3+O2↑
156 32
x 7.2kg
156/32=x/7.2kg
x=35.1kg
答:该潜水艇中每天需要过氧化钠35.1kg.
点评:此题为综合实验题,考察了多个知识点.

练习册系列答案
相关题目
 钙是维持人体正常功能所必需的元素,如图所示为某种补钙剂说明书的一部分.某校化学兴趣小组同学取10片该种钙片于烧杯中,再向其中加入20g稀盐酸,其中的碳酸钙跟盐酸恰好完全反应(其他成分与盐酸不反应),烧杯内物质的质量变为23.24g.请你计算:
钙是维持人体正常功能所必需的元素,如图所示为某种补钙剂说明书的一部分.某校化学兴趣小组同学取10片该种钙片于烧杯中,再向其中加入20g稀盐酸,其中的碳酸钙跟盐酸恰好完全反应(其他成分与盐酸不反应),烧杯内物质的质量变为23.24g.请你计算: