题目内容
3.小组在实验室进行关于气体的实验,所用的部分仪器如下图所示.
(1)甲同学用双氧水制取氧气,发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选择的收集装置是D或E(从A到E中选),用带火星的木条检验D收集满氧气.
(2)乙同学用氯酸钾和二氧化锰为原料制取氧气,应选择的发生装置是A,若用F装置收集氧气,气体应从b端进入.该同学发现产生的气体能使带火星的木条复燃并有刺激性气味,下列分析不合理的是ad.
a.反应中氧气的物理性质发生了变化
b.此时得到的气体一定是混合物
c.只加热氯酸钾,若生成的气体无气味,说明刺激性气味一定与二氧化锰有关
d.可能是生成的氧气与残留在发生装置中的空气在加热的条件下反应生成了新物质.
(3)实验室制取二氧化碳气体选择装置B,若用F装置除去二氧化碳中混有的氯化氢气体,气体应从a端进入.
分析 (1)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,氧气密度比空气大,不易溶于水,氧气有助燃性进行分析;
(2)根据实验室用氯酸钾和二氧化锰制取氧气的反应物是固体,反应条件是加热,氧气密度比水小,依据反应原理分析实验中的不合理原因;
(3)根据实验室制取二氧化碳的反应物是固体和液体,反应条件生成常温,洗气应该是长进短出进行分析.
解答 解:(1)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,氧气密度比空气大,不易溶于水,所以选择的收集装置是D或E,氧气有助燃性,所以用带火星的木条检验D收集满氧气;
(2)实验室用氯酸钾和二氧化锰制取氧气的反应物是固体,反应条件是加热,所以应选择的发生装置是A,氧气密度比水小,所以用F装置收集氧气,气体应从b端进入,如产生的气体能使带火星的木条复燃并有刺激性气味,原因不合理的是:反应中氧气的物理性质发生了变化、可能是生成的氧气与残留在发生装置中的空气在加热的条件下反应生成了新物质等,故选:ad;
(3)实验室制取二氧化碳的反应物是固体和液体,反应条件生成常温,所以发生装置选B,洗气应该是长进短出,所以用F装置除去二氧化碳中混有的氯化氢气体,气体应从a端进入.
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,E,带火星的木条;
(2)A,b,ad;
(3)B,a.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.如图实验操作不正确的是( )
| A. | 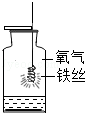 铁丝在氧气中燃烧 | B. | 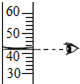 读取液体的体积 | ||
| C. | 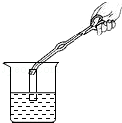 测溶液的PH | D. | 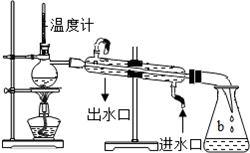 制取蒸馏水 |
15.下列变化属于化学变化的是( )
| A. | 硫在氧气中燃烧 | B. | 灯泡通电发光 | C. | 食盐水的蒸发 | D. | 湿衣服晾干 |


 过氧乙酸是一种消毒剂,其结构如图所示;请回答下列问题:
过氧乙酸是一种消毒剂,其结构如图所示;请回答下列问题: