题目内容
4. 某同学向一定质量AgNO3和Cu(NO3)2的混合溶液中加人固体Zn,测得反应过程中溶液质量与加入Zn的质量关系如图所示.请回答下列问题:
某同学向一定质量AgNO3和Cu(NO3)2的混合溶液中加人固体Zn,测得反应过程中溶液质量与加入Zn的质量关系如图所示.请回答下列问题:(1)若取a点溶液,滴加稀盐酸,可观察到的现象为产生白色沉淀;
(2)c点溶液中的溶质为Zn(NO3)2;
(3)d点的固体为Ag、Cu、Zn.
分析 根据金属与盐溶液的反应进行分析,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答即可.
解答 解:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,锌先与硝酸银反应,当硝酸银完全反应后,锌再与硝酸铜反应.
Zn+2AgNO3=Zn(NO3)2+2Ag
65 216
析出银的过程是溶液质量减少的过程,
Zn+Cu(NO3)2=Zn(NO3)2+Cu
65 64
析出铜的过程是溶液质量增加的过程.
由此可知:
(1)由图象可知,若取a点溶液,溶液中含有未完全反应的硝酸银,滴加稀盐酸,可观察到的现象为产生白色沉淀;
(2)由图象可知,c点溶液中的硝酸铜恰好完全反应,溶液中的溶质为:Zn(NO3)2;
(3)由图象可知,d点加入的锌是过量的,溶液中银、铜全部置换出来了,固体为:Ag、Cu、Zn.
故答为:(1)产生白色沉淀;(2)Zn(NO3)2;(3)由Ag、Cu、Zn.
点评 本题考查了金属活动性顺序的应用,要求学生熟悉金属的活动性顺序表,能利用活动性判断反应的发生,还要结合坐标分析各段的意义.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.推理是科学学习中常用的思维方法,下列推理中,正确的是( )
| A. | 离子是带电的粒子,故带电的粒子一定都是离子 | |
| B. | 碳酸钠溶液呈碱性,所以该溶液中一定含有氢氧根离子 | |
| C. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 | |
| D. | 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 |
12.在氯化铜和氯化亚铁的混合溶液中加入一定量的锌粉,充分反应后,过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.正确的是( )
| A. | 滤液中一定含有氯化锌和氯化亚铁,可能含有氯化铜 | |
| B. | 滤出的固体中一定含有铜,可能含有锌和铁 | |
| C. | 滤出的固体中一定含有铜,一定不含锌,可能含有铁 | |
| D. | 滤液中一定含有氯化锌,氯化亚铁,氯化铜 |
19.下列各组物质中,不可能为同一个反应的生成物的是( )
| A. | 氯化钠、水 | B. | 氯化钙、碳酸钾 | ||
| C. | 氯化钠、水、二氧化碳 | D. | 碳酸钙、氢氧化钠 |
16.兴趣小组的同学对实验室中存放的一瓶熟石灰固体试剂进行了如下实验探究活动,请你参与他们的探究活动,并回答有关问题.
(1)小组间学认为:该试剂已经变质,因为熟石灰在空气中能发生反应:Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
(2)为检验熟石灰是否变质,小组同学进行了下列实验:取少量熟石灰样品放入洁净的烧杯中,然后向烧杯中加人一定量的稀盐酸,观察到有气泡产生(填写实验现象),最终固体全部消失,得到无色溶液.证明熟石灰样品已变质.
(3)实验(2)所得无色溶液中溶质的成分是什么呢?
【作出猜想】
【讨论】小组同学一致认为猜想四不合理,理由是氯化氢和氢氧化钙不能共存.
【查阅资料】氯化钙溶液呈中性.
【实验验证】
小明的方案:取少量烧杯中的溶液,向溶液中滴加几滴酚酞溶液,若溶液不变色,证明猜想三正确.小组同学认为该方案不合理.理由是滴酚酞溶液遇酸性或中性溶液都不变色.
小阳的方案:取少量烧杯中的溶液,向其中滴加碳酸钠溶液,因氢氧化钙与碳酸钠溶液能反应生成白色沉淀,证明猜想二正确.该方案也被小组同学否定了,否定的原因是Na2CO3+CaCl2=CaCO3↓+2NaCl(用化学方程式表示).
小组合议的方案:取少量烧杯中的溶液,用pH试纸测其pH约为4,证明猜想三正确.他们测定pH的正确操作是将一小片pH试纸放在表面皿上,用玻璃棒或胶头滴管将待测液滴在试纸上,再将变色的试纸与标准比色卡对照读出数值.
【反思】在实验探究过程中,实验方案必须要科学合理,才能得出正确的结论.
(1)小组间学认为:该试剂已经变质,因为熟石灰在空气中能发生反应:Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
(2)为检验熟石灰是否变质,小组同学进行了下列实验:取少量熟石灰样品放入洁净的烧杯中,然后向烧杯中加人一定量的稀盐酸,观察到有气泡产生(填写实验现象),最终固体全部消失,得到无色溶液.证明熟石灰样品已变质.
(3)实验(2)所得无色溶液中溶质的成分是什么呢?
【作出猜想】
| 猜想一 | 猜想二 | 猜想三 | 猜想四 |
| 只有氯化钙 | 氢氧化钙和氯化钙 | 氯化氢和氯化钙 | 氯化氢、氢氧化钙和氯化钙 |
【查阅资料】氯化钙溶液呈中性.
【实验验证】
小明的方案:取少量烧杯中的溶液,向溶液中滴加几滴酚酞溶液,若溶液不变色,证明猜想三正确.小组同学认为该方案不合理.理由是滴酚酞溶液遇酸性或中性溶液都不变色.
小阳的方案:取少量烧杯中的溶液,向其中滴加碳酸钠溶液,因氢氧化钙与碳酸钠溶液能反应生成白色沉淀,证明猜想二正确.该方案也被小组同学否定了,否定的原因是Na2CO3+CaCl2=CaCO3↓+2NaCl(用化学方程式表示).
小组合议的方案:取少量烧杯中的溶液,用pH试纸测其pH约为4,证明猜想三正确.他们测定pH的正确操作是将一小片pH试纸放在表面皿上,用玻璃棒或胶头滴管将待测液滴在试纸上,再将变色的试纸与标准比色卡对照读出数值.
【反思】在实验探究过程中,实验方案必须要科学合理,才能得出正确的结论.
13. 硝酸钾与氯化钾的溶解度曲线如图所示.下列说法错误的是( )
硝酸钾与氯化钾的溶解度曲线如图所示.下列说法错误的是( )
 硝酸钾与氯化钾的溶解度曲线如图所示.下列说法错误的是( )
硝酸钾与氯化钾的溶解度曲线如图所示.下列说法错误的是( )| A. | 硝酸钾和氯化钾的溶解度都是随温度升高而增大 | |
| B. | 20℃时,硝酸钾和氯化钾的溶解度相等 | |
| C. | 40℃时,硝酸钾溶液的溶质质量分数比氯化钾大 | |
| D. | 60℃时,55克硝酸钾溶于50水中,恰好形成饱和溶液 |

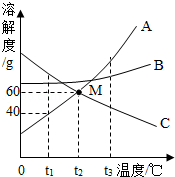 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答: