题目内容
20.根据下列实验,回答有关问题:(1)铁钉与硫酸铜溶液反应.将几根铁钉用砂纸打磨干净,浸到盛有适量硫酸铜溶液的锥形瓶中,待反应一段时间后,观察到溶液的颜色变化是溶液由蓝色变成浅绿色,化学方程式为Fe+CuSO4═FeSO4+Cu.
(2)镁条在空气中燃烧.取一根用砂纸打磨干净的长镁条和一个石棉网,将它们一起放在托盘天平上称量,其质量为m1;在石棉网上方将镁条点燃,燃烧后的产物全部落在石棉网上;再将镁条燃烧后的产物与石棉网一起放在托盘天平上称量,其质量为m2.
①观察镁条燃烧的现象是发出耀眼的白光,生成白色固体,化学反应的方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
②当m2<m1时,请分析这样的实验结果:镁条的燃烧会生成大量的白烟散失到空气中,使燃烧后的剩余固体质量有可能比反应的固体质量小.
分析 (1)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(2)根据镁和氧气在点燃的条件下生成氧化镁,镁条的燃烧会生成大量的白烟散失到空气中使燃烧后的剩余固体质量减小进行分析.
解答 解:(1)铁和硫酸铜反应生成硫酸亚铁和铜,所以观察到溶液的颜色变化是溶液由蓝色变成浅绿色,化学方程式为:Fe+CuSO4═FeSO4+Cu;
(2)镁和氧气在点燃的条件下生成氧化镁,所以观察镁条燃烧的现象是:发出耀眼的白光,生成白色固体,化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
镁条的燃烧会生成大量的白烟散失到空气中使燃烧后的剩余固体质量减小,所以m2<m1.
故答案为:(1)溶液由蓝色变成浅绿色,Fe+CuSO4═FeSO4+Cu;
(2)发出耀眼的白光,生成白色固体,2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
镁条的燃烧会生成大量的白烟散失到空气中,使燃烧后的剩余固体质量有可能比反应的固体质量小.
点评 本题是对质量守恒定律的考查,解题的关键是对质量守恒定律微观及宏观意义的掌握.

练习册系列答案
相关题目
11.如图为元素周期表第三周期的一部分,据此判断下列说法中正确的是( )


| A. | 硅、磷、硫、氯四种元素都属于非金属元素 | |
| B. | 不同元素本质区别是最外层电子数不同 | |
| C. | 硫元素的相对原子质量是32.06g | |
| D. | 磷原子的核内中子数是15 |
15.某种锂电池的总反应可表示为:Li+MnO2=LiMnO2.以下说法正确的是( )
| A. | LiMnO2为新型氧化物 | B. | 该反应属于化合反应 | ||
| C. | 该反应中锰元素的化合价没有改变 | D. | 此反应中,二氧化锰是催化剂 |
5.下列说法正确的是( )
| A. | 不饱和溶液和饱和溶液在一定条件下可相互转化 | |
| B. | 饱和溶液一定是浓度大的溶液 | |
| C. | 饱和溶液降低温度一定会析出晶体 | |
| D. | 不饱和溶液一定比饱和溶液的质量分数小 |
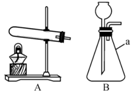
12.根据如图中的实验装置,回答问题:
(1)仪器“a”的名称是锥形瓶.
(2)实验室用加热高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,,发生装置是A(填字母序号,下同).
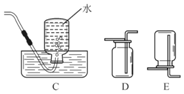
(3)实验室用石灰石和稀盐酸反应制取二氧化碳,收集装置是D,选择该装置进行收集的理由是二氧化碳能溶于水,密度大于空气密度;若二氧化碳中混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从 F 装置的② 端口(填“①”或“②”)通入.
| 发生装置 | 收集装置 | 洗气装置 |
 |  | 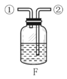 |
(2)实验室用加热高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,,发生装置是A(填字母序号,下同).
(3)实验室用石灰石和稀盐酸反应制取二氧化碳,收集装置是D,选择该装置进行收集的理由是二氧化碳能溶于水,密度大于空气密度;若二氧化碳中混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从 F 装置的② 端口(填“①”或“②”)通入.
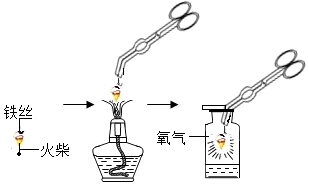 氧气是初中化学中的常见气体,请结合有关知识回答下列问题:
氧气是初中化学中的常见气体,请结合有关知识回答下列问题: