题目内容
【题目】碳酸氢钠是化学实验中常见的药品,在工业上有很多制取方法。重庆一中兴趣小组的同学 们查询资料发现了一种“气相固碳法”:向氢氧化钠溶液中通入过量的CO2气体。
整理资料:Ⅰ、过量CO2通入NaOH溶液,发生两步反应:
①_________________________________(写出化学方程式);
②Na2CO3 +H2O + CO2=2NaHCO3
Ⅱ、碳酸钠和碳酸氢钠的溶解度表(部分)
温度/℃ | 0 | 15 | 20 | 30 |
Na2CO3 溶解度/g | 7.1 | 13.25 | 21.8 | 39.7 |
NaHCO3 溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 |
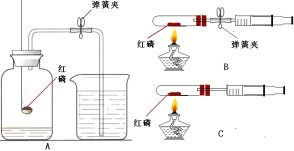
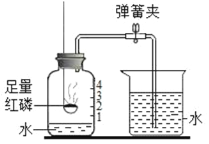
15℃时,将10g氢氧化钠固体完全溶解溶于100g水中(如图1),而后匀速的通入二氧化碳气体,同时用pH计测定溶液的pH值变化(如图2)。

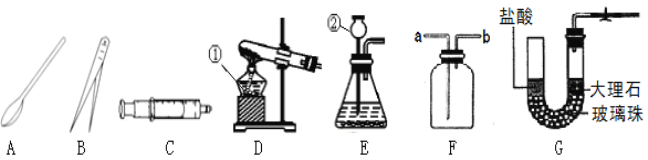
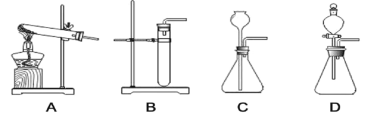
(1)图 1 所示实验中,产生 CO2 的装置应该选择:_____(填序号);
(2)为了确定M处溶液的溶质成分,取少量样品于试管中,进行如下实验:
步骤 | 加入试剂 | 实验现象 | 实验结论 |
① | 加入_______溶液 | 溶液变红 | NaOH和Na2CO3 |
② | 加入过量_______溶液 | ______ |
(3)实验中,t2后溶液的pH基本不变,则此时烧杯中观察到的现象是_____。
【答案】2NaOH+CO2═Na2CO3+H2O BCD 无色酚酞 氯化钙 有白色沉淀生成,且红色不消失 有不溶物析出
【解析】
I、二氧化碳和氢氧化钠反应生成碳酸钠和水,化学方程式为:2NaOH+CO2═Na2CO3+H2O;
II、(1)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以图1所示实验中,产生CO2的装置应该选择BCD;
(2)碳酸钠、氢氧化钠溶液显碱性,能使无色酚酞变红色,碳酸钠和氯化钙反应生成碳酸钙沉淀;
(3)实验过程中,溶液中溶解过量的二氧化碳后,二氧化碳与溶液中的碳酸钠反应,生成碳酸氢钠,因为碳酸钠在水中溶解度大,碳酸氢钠在水中溶解度小,碳酸氢钠达到一定量时会析出。

【题目】俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于编制出了现代元素周期表的雏形表。下表为元素周期表的部分元素的部分信息,利用下表回答相关问题。
第一周期 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
第二周期 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
第三周期 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)请画出16号元素的原子结构示意图__________,化学反应中该原子比较容易__________电子变成离子;
(2)![]() 表示的是________,其与17号元素形成的化合物是________
表示的是________,其与17号元素形成的化合物是________
(3)同一纵列元素原子的结构特点是________________
(4)上表中第二、三周期元素最外层电子数的变化规律是___________