题目内容
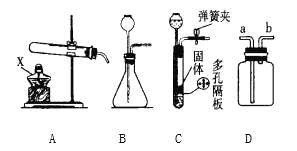
【题目】课堂上老师利用如图所示的装置演示硫在氧气中燃烧的实验,回答下列问题
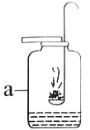
(1)实验现象是:________________________;
(2)水的作用是___________________________;
(3)仪器a的名称是__________;
(4)写出该实验的化学反应方程式:____________________________________。
【答案】发出蓝紫色火焰、放热、生成有刺激性气味的气体 吸收二氧化硫,防止空气污染 集气瓶 S+O2![]() SO2
SO2
【解析】
(1)硫在氧气中燃烧时,发出蓝紫色火焰、放热、生成有刺激性气味的气体;
(2)由于二氧化硫有毒性,必须吸收以防止空气污染,根据二氧化硫溶解于水及与水反应生成亚硫酸的性质,可用水来吸收;
(3)据图可知仪器a是集气瓶;
(4)硫在氧气中燃烧的反应物是硫和氧气,生成物是二氧化硫,反应条件是点燃,所以方程式是:S+O2![]() SO2。
SO2。

【题目】碳酸氢钠是化学实验中常见的药品,在工业上有很多制取方法。重庆一中兴趣小组的同学 们查询资料发现了一种“气相固碳法”:向氢氧化钠溶液中通入过量的CO2气体。
整理资料:Ⅰ、过量CO2通入NaOH溶液,发生两步反应:
①_________________________________(写出化学方程式);
②Na2CO3 +H2O + CO2=2NaHCO3
Ⅱ、碳酸钠和碳酸氢钠的溶解度表(部分)
温度/℃ | 0 | 15 | 20 | 30 |
Na2CO3 溶解度/g | 7.1 | 13.25 | 21.8 | 39.7 |
NaHCO3 溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 |
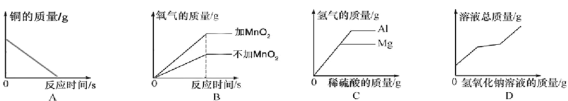
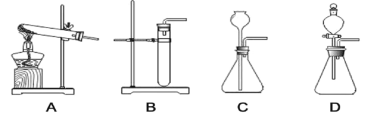
15℃时,将10g氢氧化钠固体完全溶解溶于100g水中(如图1),而后匀速的通入二氧化碳气体,同时用pH计测定溶液的pH值变化(如图2)。

(1)图 1 所示实验中,产生 CO2 的装置应该选择:_____(填序号);
(2)为了确定M处溶液的溶质成分,取少量样品于试管中,进行如下实验:
步骤 | 加入试剂 | 实验现象 | 实验结论 |
① | 加入_______溶液 | 溶液变红 | NaOH和Na2CO3 |
② | 加入过量_______溶液 | ______ |
(3)实验中,t2后溶液的pH基本不变,则此时烧杯中观察到的现象是_____。
【题目】同学们从山上采集到一种石灰石,他们取100g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
反应后固体的质量m∕g | 100 | 92 | 84 | 78 | 72 | 67 | 67 |
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为__________g。
(2)求该石灰石中CaCO3的质量分数(即CaCO3在石灰石中所占的百分含量),写出计算过程________。
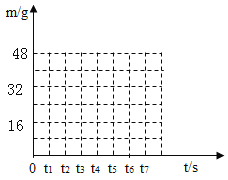
(3)请在如图所示的坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线________。