题目内容
6. 如图所示是钠元素和氯元素在元素周期表中的信息和三种粒子的结构示意图.请回答下列问题:
如图所示是钠元素和氯元素在元素周期表中的信息和三种粒子的结构示意图.请回答下列问题:(1)氯的核电荷数是17;钠原子的相对原子质量为22.99.
(2)钠元素与氯元素的最本质区别是①不同(填序号).
①质子数 ②核外电子数 ③最外层电子数
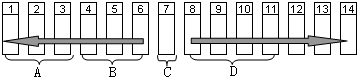
(3)在图B中,该微粒属于①(填序号).
①原子 ②分子 ③离子
(4)图C中的微粒有3个电子层;最外层电子数是7,它在化学反应中容易(填“失去”或“得到”)一个电子,形成的离子,其离子符号是Cl-.
(5)在地壳中,含量排在前四位的元素是氧、硅、铝、铁.
分析 (1)根据元素周期表的信息来分析;
(2)根据元素的概念来分析;
(3)根据质子数与核外电子数的关系来分析;
(4)根据原子结构示意图的信息以及离子符号的写法来分析;
(5)根据地壳中各元素的含量来分析.
解答 解:(1)由元素周期表的信息可知,氯的核电荷数为17,钠原子的相对原子质量为22.99;故填:17;22.99;
(2)元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,所以钠元素与氯元素的最本质区别是质子数(即核电荷数)不同.故填:①;
(3)该粒子核内的质子数=核外的电子数,是原子;故填:①;
(4)由C的原子结构示意图可知,其核外有3个电子层,最外层有7个电子,在化学反应中易得到一个电子,而带上一个单位的负电荷;故填:3;7;得到;Cl-;
(5)地壳中元素含量由高到低前五种依次为氧、硅、铝、铁、钙,故填:氧;硅;铝;铁.
点评 本题难度不大,掌握元素周期表的信息、粒子结构示意图的含义等是正确解答本题的关键.

练习册系列答案
相关题目
10.用20%的食盐溶液50g与20%的食盐溶液50mL混合,混合后溶液的质量分数是( )
| A. | 10% | B. | 20% | C. | 40% | D. | 无法计算 |
18.原来用于烧煤气的灶,现改烧甲烷,则下列对灶的改进措施正确的是( )
| A. | 同时减少空气和燃料气入口 | B. | 同时增大空气和燃料气入口 | ||
| C. | 增大空气入口,减少燃料气入口 | D. | 减少空气入口,增大燃料气入口 |
16.对甲状腺肿大的病人医生常建议多吃海带,这是因为海带中含有较丰富的( )
| A. | 铁元素 | B. | 氟元素 | C. | 硒元素 | D. | 碘元素 |

 小明欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸氢钠反应”为研究对象,设计的实验装置如图所示.化学反应前烧杯里有50g稀盐酸,试管里有2g碳酸氢钠粉末;化学反应时将碳酸氢钠粉末倒入稀盐酸,试管再放回烧杯.
小明欲通过化学实验证明“质量守恒定律”,确定以“稀盐酸与碳酸氢钠反应”为研究对象,设计的实验装置如图所示.化学反应前烧杯里有50g稀盐酸,试管里有2g碳酸氢钠粉末;化学反应时将碳酸氢钠粉末倒入稀盐酸,试管再放回烧杯.