题目内容
1.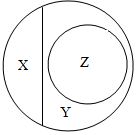 分类是研究物质的常用方法.右图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )
分类是研究物质的常用方法.右图是纯净物、单质、化合物、氧化物之间关系的形象表示,若整个大圈表示纯净物,则下列物质属于Z范围的是( )| A. | 红磷 | B. | 干冰 | C. | 氯酸钾 | D. | 食盐水 |
分析 物质包括混合物和纯净物,纯净物包括单质和化合物,化合物包括酸、碱、盐、氧化物,根据它们之间的包含关系分析.
解答 解:由图中信息可知,x属于单质;y属于化合物;z属于氧化物.
A、红磷属于单质,故A错;
B、干冰是由碳元素和氧元素组成,属于氧化物,故B正确;
C、氯酸钾由三种元素组成,属于化合物,故C错;
D、食盐水中含有氯化钠和水,属于混合物,故D错.
故选B.
点评 解答本题要掌握物质的分类方法方面的知识,只有这样才能对各种物质进行正确的分类.

练习册系列答案
相关题目
11.下列说法正确的是( )
| A. | 等质量的二氧化硫和三氧化硫中硫元素的质量比为5:4 | |
| B. | 等质量的乙醇和甲烷完全燃烧,生成的二氧化碳和水的质量均相等 | |
| C. | 等质量的高锰酸钾和氯酸钾分别受热完全分解,生成氧气质量相等 | |
| D. | 等质量的碳酸钠和碳酸氢钠分别与足量稀盐酸充分反应,生成二氧化碳质量相等 |
12.生铁是铁和碳的合金,为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品6.0g,放入烧杯中,向其中加入65.0g稀硫酸,恰好完全反应(Fe+H2SO4═FeSO4+H2↑)(假设杂质不参与反应),测得的实验数据如下:
请你完成有关计算(结果保留一位小数):
(1)硫酸中H:S:O的元素质量比是1:16:24.
(2)反应放出的氢气是0.2g.
(3)生铁样品中铁的质量分数是多少?
(4)反应后所得溶液中溶质的质量分数是多少?
| 反应前 | 反应后 | |
| 烧杯及其中物质的质量 | 97.0g | 96.8g |
(1)硫酸中H:S:O的元素质量比是1:16:24.
(2)反应放出的氢气是0.2g.
(3)生铁样品中铁的质量分数是多少?
(4)反应后所得溶液中溶质的质量分数是多少?
9.下面对有关实验的设计与解释,不合理的是( )
| 实验内容 | 试剂与方法 | 结论与解释 | |
| A | 分离CaCO3和CaO | 加水溶解、过滤 | CaO溶于水 |
| B | 除去BaSO4中的BaCO3 | 加稀盐酸、过滤 | BaCO3溶于稀盐酸 |
| C | 鉴别NaOH、Na2SO4 | 滴加酚酞试液 | NaOH溶液显碱性 |
| D | 检验溶液中的Mg2+ | 滴加NaOH溶液 | Mg(OH)2不溶于水 |
| A. | A | B. | B | C. | C | D. | D |
13.二氧化碳在一定条件下可转化为重要的化工原料乙烯,其反应的微观过程如图所示.
下列有关叙述中正确的是( )

下列有关叙述中正确的是( )
| A. | 碳原子结构示意图为 | B. | 二氧化碳和乙烯均属于氧化物 | ||
| C. | 反应前后原子种类和数目均不变 | D. | 参加反应两种分子的个数比为4:1 |
 蛋白粉是由大豆蛋白、酪蛋白、乳清蛋白或上述几种蛋白混合制成的粉剂,其用途是为营养不良或疾病导致蛋白质缺乏的人群补充营养.请回答:
蛋白粉是由大豆蛋白、酪蛋白、乳清蛋白或上述几种蛋白混合制成的粉剂,其用途是为营养不良或疾病导致蛋白质缺乏的人群补充营养.请回答:
