题目内容
18.分析推理是化学学习中常用的思维方法,下列分析推理正确的是( )| A. | 浓硫酸具有吸水性,所以浓盐酸也具有吸水性 | |
| B. | 酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 | |
| C. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| D. | H2O和H2O2的分子构成不同,所以它们的化学性质不同 |
分析 A、根据酸的性质解答;
B、根据酸雨的概念解答;
C、根据带电的微粒解答;
D、根据物质的结构与性质的关系解答.
解答 解:A、浓盐酸不具有吸水性,错误;
B、pH小于7的雨水不一定是酸雨,错误;
C、离子是带电荷的微粒,带电荷的微粒不一定是离子比如原子核,错误;
D、H2O和H2O2的分子构成不同,所以它们的化学性质不同,正确;
故选D.
点评 本题考查的是常见的物质的性质以及物质的微观构成的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
8.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和硫酸两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和硫酸两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
13.下列变化属于化学变化的是( )
| A. | 湿衣服晾干 | B. | 冰雪融化 | C. | 香水挥发 | D. | 菜刀生锈 |
3.下列四组溶液,仅用组内物质就能鉴别出来且均为无色溶液的是( )
| A. | HCl FeCl3 KOH ZnSO4 | B. | NH4NO3 Ba(OH)2 H2SO4 MgCl2 | ||
| C. | NaCl MgCl2 K2SO4 CuSO4 | D. | K2CO3 Na2SO4 BaCl2 NaOH |
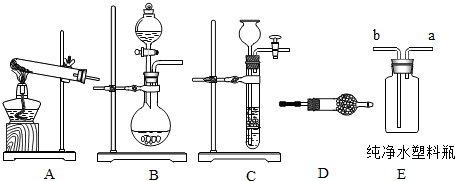
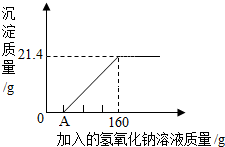 某化工厂的废水中只含有稀盐酸和氯化铁,小敏采集了该废水样品95.4g,并向其中滴加20%的氢氧化钠溶液至恰好完全反应,测得所加入的氢氧化钠溶液质量与反应生成的沉淀质量关系如图所示,已知上述反应后所得溶液在常温下为不饱和溶液,求该溶液中溶质的质量分数.
某化工厂的废水中只含有稀盐酸和氯化铁,小敏采集了该废水样品95.4g,并向其中滴加20%的氢氧化钠溶液至恰好完全反应,测得所加入的氢氧化钠溶液质量与反应生成的沉淀质量关系如图所示,已知上述反应后所得溶液在常温下为不饱和溶液,求该溶液中溶质的质量分数.