题目内容
15.化学与生活息息相关,请你用所学化学知识回答以下生活中的问题.
(1)某品牌矿物质水标签的部分内容如图1所示.
①该矿泉水中至少含有5种非金属元素;
②硫酸镁中阴离子的符号是SO42-;
③镁离子的结构示意图是图2中的C(填序号);
④可以用肥皂水来检验该矿泉水是硬水还是软水.
(2)请选用H、O、N三种元素中的一种或几种填写符合下列要求的化学式(各写一个):
①可用于炼钢的气体是O2;
②可用来填充探空气球的气体是H2;
③人体中含量最多的物质H2O;
④食品包装中作保护气的气体N2.
分析 (1)①根据某品牌矿物质水标签,可知含有:氯化钾、硫酸镁、偏硅酸,则可判断其元素种类;
②离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
③根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
④根据区分硬水和软水用肥皂水进行回答;
(2)首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可.
解答 解:(1)①由氯化钾、硫酸镁、偏硅酸,则可判断其含有非金属元素种类为:氯、硫、氧、硅、氢元素;故填:5;
②硫酸镁中的阴离子是硫酸根离子,故填:SO42-;
③A、质子数=核外电子数=12,为镁原子;B、质子数=17,核外电子数=18,质子数<核外电子数,为阴离子;C、质子数=12,核外电子数=10,质子数>核外电子数,为镁离子.故填:C;
④肥皂水在硬水中的泡沫较少,在软水中的泡沫较多,根据现象不同,可以鉴别软水和硬水;故填:肥皂水;
(2)①氧气用于富氧炼钢,故填:O2;
②氢气的密度非常小,常用于填充探空气球,故填:H2;
③人体内含量最多的物质是水,故填:H2O;
④氮气的性质稳定,经常做食品的保护气充入食品包装袋内,故填:N2
点评 在解此类题时,首先要弄清考查的知识点,然后再结合学过的知识进行解答,此类题一般难度小,便于作答.

练习册系列答案
相关题目
18.下列有关化学符号的说法不正确的是( )
| A. | “5Fe”只具有微观意义 | |
| B. | 表示+2价的钙元素$\stackrel{+2}{Ca}$ | |
| C. | 化学式“H2O”可以表示一个水分子 | |
| D. | “3SO42-”中“2-”表示三个硫酸根离子带二个负电荷 |
3.如表为元素周期表中某一周期元素的原子结构示意图.请回答下列问题:
(1)铝元素在元素周期表中的更多信息如图,有关铝元素及其原子结构的下列说法中,错误的是D
A.铝的原子序数为13
B.铝原子在反应中容易失去3个电子
C.铝属于金属元素
D.铝的相对原子质量为26.98克
(2)表中磷原子的核电荷数X=15.
(3)表中具有相对稳定结构的元素是氩.
(4)在化学反应中,每个铝原子失去电子形成铝离子的化学符号是Al3+.
(5)上述元素在周期表中处于第三周期.
| 元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 元素符号 | Na | Mg | Al | Si | p | S | Cl | Ar |
| 原子结构 示意图 |  |  |  |  | 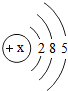 |  |  |  |

A.铝的原子序数为13
B.铝原子在反应中容易失去3个电子
C.铝属于金属元素
D.铝的相对原子质量为26.98克
(2)表中磷原子的核电荷数X=15.
(3)表中具有相对稳定结构的元素是氩.
(4)在化学反应中,每个铝原子失去电子形成铝离子的化学符号是Al3+.
(5)上述元素在周期表中处于第三周期.
20.下列变化中不包含化学变化的是( )
| A. |  纸张燃烧 | B. |  电热壶内水沸腾 | C. |  葡萄酒变酸 | D. |  白菜腐烂 |
4.研究盐类物质的性质时,甲、乙、丙三位同学分别向NaHCO3溶液中滴加石灰水,均产生白色沉淀.他们分别设计实验方案,对自己过滤后的滤液中溶质的成分进行如下探究.
【实验准备】
用一定溶质的质量分数的NaHCO3溶液、NaOH溶液和Na2CO3溶液进行如下实验,为设计实验方案提供参考.
表中的现象Ⅰ为溶液变红;现象Ⅱ为产生蓝色沉淀,对应反应的化学方程式是CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
【查阅资料】
(1)氯化钙溶液显中性.
(2)滤液中所含的溶质有以下几种可能:
①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④Na2CO3和NaHCO3;⑤Na2CO3和NaOH
实验及分析】
甲同学:取少量滤液于试管中,滴加过量的稀盐酸,产生大量无色气泡,则滤液中的溶质是Na2CO3.
乙同学:取少量滤液于试管中,向其中通入少量CO2,产生白色沉淀,则滤液中的溶质是NaOH和Ca(OH)2.
丙同学:分别取少量滤液于两支试管中,向一支试管中滴加CaCl2溶液,有白色沉淀产生;将另一支试管中的滤液加热至沸腾,将产生的气体通入澄清石灰水,澄清石灰水变浑浊,则滤液中的溶质是Na2CO3和NaHCO3.
反思与评价】
(1)老师认为乙、丙同学的实验方案和结论合理.
①丙同学的实验中,加入CaCl2溶液的目的是检验Na2CO3.
②根据乙同学的结论,NaHCO3溶液与澄清石灰水反应的化学方程式是NaHCO3+Ca(OH)2=NaOH+CaCO3↓+H2O.
(2)老师认为甲同学的实验方案和结论存在不足.丁同学通过以下实验帮助甲同学确认了滤液中溶质的成分.
(3)结合此次探究活动,你认为下列说法正确的是abd(填字母序号).
a.盐溶液可能显碱性
b.化学反应的产物与反应物的量有关
c.碱和盐反应一定生成另外一种碱和另外一种盐
d.判断溶液混合后的成分不仅要考虑产物,还要考虑反应物是否过量.
【实验准备】
用一定溶质的质量分数的NaHCO3溶液、NaOH溶液和Na2CO3溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入酚酞溶液 | 溶液变红 | 现象Ⅰ | 溶液变红 |
| 加入CuSO4溶液 | 产生气泡和蓝色沉淀 | 现象Ⅱ | 产生气泡和蓝色沉淀 |
| 加入CaCl2溶液 | 无明显变化 | 无明显变化 | 产生白色沉淀 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
【查阅资料】
(1)氯化钙溶液显中性.
(2)滤液中所含的溶质有以下几种可能:
①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④Na2CO3和NaHCO3;⑤Na2CO3和NaOH
实验及分析】
甲同学:取少量滤液于试管中,滴加过量的稀盐酸,产生大量无色气泡,则滤液中的溶质是Na2CO3.
乙同学:取少量滤液于试管中,向其中通入少量CO2,产生白色沉淀,则滤液中的溶质是NaOH和Ca(OH)2.
丙同学:分别取少量滤液于两支试管中,向一支试管中滴加CaCl2溶液,有白色沉淀产生;将另一支试管中的滤液加热至沸腾,将产生的气体通入澄清石灰水,澄清石灰水变浑浊,则滤液中的溶质是Na2CO3和NaHCO3.
反思与评价】
(1)老师认为乙、丙同学的实验方案和结论合理.
①丙同学的实验中,加入CaCl2溶液的目的是检验Na2CO3.
②根据乙同学的结论,NaHCO3溶液与澄清石灰水反应的化学方程式是NaHCO3+Ca(OH)2=NaOH+CaCO3↓+H2O.
(2)老师认为甲同学的实验方案和结论存在不足.丁同学通过以下实验帮助甲同学确认了滤液中溶质的成分.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量滤液于试管中,加入过量CaCl2溶液 ②过滤,向滤液中滴加CuSO4溶液 | ①有白色沉淀生成 ②只产生蓝色沉淀,无气泡 | 滤液中的溶质是Na2CO3和NaOH |
a.盐溶液可能显碱性
b.化学反应的产物与反应物的量有关
c.碱和盐反应一定生成另外一种碱和另外一种盐
d.判断溶液混合后的成分不仅要考虑产物,还要考虑反应物是否过量.


