题目内容
6.实验室用氯酸钾和二氧化锰的混合物共8g制取氧气.加热到不再产生氧气时,将剩余固体冷却后称量,质量为6.08g.求:(1)产生氧气的质量
(2)原混合物中氯酸钾的质量.
分析 根据氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气;根据质量守恒定律,固体减少的质量即生成的氧气的质量,据此根据反应的化学方程式列式计算出参加反应氯酸钾的质量,进而计算出反应前固体混合物中氯酸钾的质量分数进行分析.
解答 解:由质量守恒定律,生成氧气的质量为8g-6.08g=1.92g;
设参加反应氯酸钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 1.92g
$\frac{245}{x}$=$\frac{96}{1.92g}$
x=4.9g
原混合物中氯酸钾的质量是4.9g.
故答案为:(1)4.8;
(2)原混合物中氯酸钾的质量是4.9g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列化学方程式书写正确的是( )
| A. | CuO+H2SO4=CuSO4+H2O | B. | 2Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | 2Fe+3CuCl2=2FeCl3+3Cu | D. | Cu+H2SO4═CuSO4+H2↑ |
15.下列有关实验现象的描述,正确的是( )
| A. | 铁在氧气中剧烈燃烧,火星四射,生成黑色四氧化三铁,并放热 | |
| B. | 硫在空气中燃烧发出明亮的蓝紫色火焰,生成一种有刺激性气味的气体 | |
| C. | 把盛有浓盐酸的试剂瓶的盖子打开后,瓶口上方会出现白雾 | |
| D. | 向生铁中加入足量稀硫酸,固体完全消失 |
8.下列四个图象的变化趋势,能正确表示对应操作的是( )


| A. | ①表示高温煅烧石灰石 | |
| B. | ②表示在等质量的Mg和Zn中分别加入溶质质量分数相等的稀盐酸 | |
| C. | ③向接近饱和的硝酸钾溶液中加入硝酸钾 | |
| D. | ④表示向HCl和CaCl2的混合溶液中逐滴加入Na2CO3溶液 |
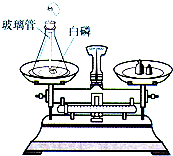 如图是测定白磷燃烧前后质量变化的实验,试回答下列问题:
如图是测定白磷燃烧前后质量变化的实验,试回答下列问题: