题目内容
19.育才中学化学社的同学欲用大理石(杂质不参与反应且难溶于水)和稀盐酸来制取二氧化碳,并回收提纯氯化钙.实验一:制取二氧化碳
(1)根据下列装置回答问题.

①装置A中发生的化学反应方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O.
②若用C装置来收集二氧化碳,二氧化碳应从①(填序号)端通入;若用B装置应来制取二氧化碳,优点为能控制反应的发生和停止.
实验二:分离提纯
(2)根据下面的流程图回答问题.

①两个步骤中都用到的玻璃仪器是玻璃棒.
②蒸发操作中,当观察到蒸发皿中出现较多固体时时,停止加热.
分析 (1)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.装置C的优点是:可以控制反应的速度;
(2)过滤用玻璃棒引流,蒸发用玻璃棒不断搅拌,以防止局部温度过高而使液体飞溅;当加热至较多固体出现时,应停止加热利用余热蒸干.
解答 解:(1)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,用C装置来收集二氧化碳,应长进短出;装置B的优点是:可以控制反应的速度;
(2)过滤用玻璃棒引流,蒸发用玻璃棒不断搅拌,以防止局部温度过高而使液体飞溅;当加热至较多固体出现时,应停止加热利用余热蒸干.
故答案为:①CaCO3+2HCl=CaCl2+H2O+CO2↑;②①、可以控制反应的速;(2)①玻璃棒;②较多固体出现时.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写及过滤、蒸发的操作等,难度比大.

练习册系列答案
相关题目
9.汉代方士发明了原始火柴--“法烛”,它用送木条上涂硫磺制成,用于引燃其他物质.下列说法正确的是( )
| A. | 送木条是易燃物,硫磺是阻燃物 | B. | “法烛”燃烧会产生刺鼻气味 | ||
| C. | 硫磺降低了松木的着火点 | D. | 吹灭“法烛”是因为隔绝了空气 |
7.下列液态物质中,属于纯净物的是( )
| A. | 液氧 | B. | 湖水 | C. | 澄清石灰水 | D. | 矿泉水 |
14.以下是黄小民同学对所学化学知识进行的比较,其中不符合实际的是( )
| A. | 反应剧烈程度:红磷燃烧比植物呼吸剧烈 | |
| B. | 硬度:金刚石比石墨大 | |
| C. | 生成物种类:化合反应比分解反应少 | |
| D. | 催化剂的质量:反应前比反应后大 |
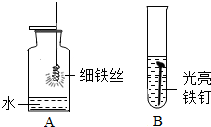 以下是初中化学有关铁的性质的一些基本实验,请回答问题.
以下是初中化学有关铁的性质的一些基本实验,请回答问题.
 如图是甲、乙两种固体物质在水中的溶解度曲线.写出你从图中能得到的信息(至少写3个)如:温度升高,甲的溶解度增大.
如图是甲、乙两种固体物质在水中的溶解度曲线.写出你从图中能得到的信息(至少写3个)如:温度升高,甲的溶解度增大.