题目内容
2.100g溶质的质量分数为10%的食盐溶液,如果使其溶质的质量分数增大一倍,应该加入食盐多少克?或者蒸发水多少克?分析 根据改变溶液的溶质质量分数有多种方法,但无论采取哪种方法,溶液的稀释计算的原则都是:在稀释前后溶液中溶质的质量不变进行分析.
解答 解:欲使质量分数增大一倍,即变为20%
若用加溶质的方法,设需加食盐的质量为x.
100g×10%+x=(100g+x)×20%,x=12.5g
若用蒸发溶剂的方法,设需蒸发水的质量为y.
(100g-y)×20%=100g×10%,y=50g
故答案为:12.5g,50g.
点评 本题是关于溶液的增浓、稀释问题的有关计算,问题的关键是稀释前后,溶液中溶质的质量不变.
解答此题注意两点:正确运用溶质质量分数的表达式;溶液稀释前后,溶质的质量保持不变.计算时熟练掌握几条规律:不论溶液的溶质质量分数为多少,取出的溶液与剩余溶液的溶质质量分数相同.要使溶液中溶质质量分数增大一倍,蒸发水的质量应等于原溶液质量的一半.要使溶液中溶质质量分数减小一半,加入水的质量应等于原溶液质量.

练习册系列答案
相关题目
12.下列化学方程式书写正确的是( )
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | CaCO3+HCl=CaCl2+CO2↑+H2O | ||
| C. | 2C+O2═2CO2 | D. | CH4+3O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
10.水是人类生活不可缺少的物质.下列有关水的叙述不正确的是( )
| A. | 水是氢和氧两种元素组成的氧化物 | |
| B. | 氢气燃烧生成水和电解水的基本反应类型相同 | |
| C. | 用肥皂水可以区分硬水和软水 | |
| D. | 无色﹑透明﹑无异味的水不一定是纯净物 |
17.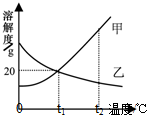 甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)
甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)
 甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)
甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是 ( )(填字母,可能有多个选项)| A. | 随着温度的升高,甲的溶解度增大,乙的溶解度减小 | |
| B. | t1℃时,30g甲加入到50g水中最多可得80g溶液 | |
| C. | t2℃,等质量的甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液质量的大小关系为:甲<乙 | |
| D. | t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲>乙 |
7.“洁厕灵”与“漂白精”不能混用,二者若混合易产生一种有毒气体X.反应原理为:NaClO+2HCl=NaCl+X↑+H2O,则X的化学式为( )
| A. | H2 | B. | ClO2 | C. | O2 | D. | Cl2 |
11.空气成分中体积分数最大的是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 水蒸气 |
