题目内容
1.硫酸亚铁可用于治疗缺铁性贫血,其中铁元素的化合价为+2,计算:(1)硫酸亚铁(FeSO4)的相对分子质量=152,其中铁元素的质量分数为36.8%;
(2)某贫血患者共需补充1.4g铁元素,服用的药物中需含硫酸亚铁多少克?
分析 根据在化合物中正负化合价代数和为零进行解答本题.
(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中元素的质量分数公式进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:根据在化合物中正负化合价代数和为零,硫酸根显-2,设铁元素的化合价是x,则:x+(-2)=0,则x=+2.
(1)硫酸亚铁的相对分子质量为56+32+16×4=152.
(2)硫酸亚铁中铁元素的质量分数$\frac{56}{152}$×100%≈36.8%.
(3)某贫血患者需补充1.4g铁,至少需要服用硫酸亚铁的质量为:1.4g÷36.8%=3.8g.
故答案为:+2;(1)152;(2)36.8%;(43)3.8g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目

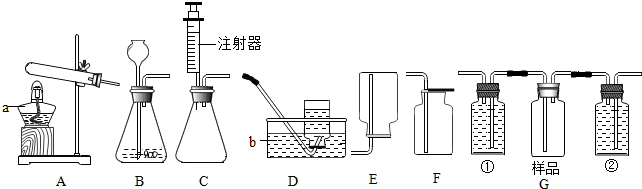
 模型可以反映客观现象简单明了地表示事物.
模型可以反映客观现象简单明了地表示事物.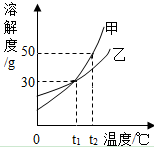 如图是甲、乙两种固体的溶解度曲线.
如图是甲、乙两种固体的溶解度曲线.