题目内容
17. 在学习氢氧化钠的性质时,老师将二氧化碳通入盛有氢氧化钠溶液的试管中,同学们没有观察到明显的现象.二氧化碳与氢氧化钠发生了反应吗?探究活动从这个疑问开始.
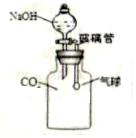
在学习氢氧化钠的性质时,老师将二氧化碳通入盛有氢氧化钠溶液的试管中,同学们没有观察到明显的现象.二氧化碳与氢氧化钠发生了反应吗?探究活动从这个疑问开始.(1)明明同学认为两者发生了反应,他设计了一种方案,如图所示,加入适量NaOH溶液后,他可观察到的小气球的变化是气球胀大,产生这种现象的原因是CO2和NaOH反应使瓶内气压减小,反应的化学方程式是CO2+2NaOH═Na2CO3+H2O.
(2)另一位同学认为这个方案还不足以证明CO2和NaOH确实发生了反应,因为NaOH溶液中有水,二氧化碳又能溶于水,为使实验方案更完善,你认为还需要做什么实验来探究这个问题?在反应后的溶液中滴入Ba(OH)2溶液(或Ca(OH)2溶液);或在反应后的溶液中滴入稀盐酸;或取两个同样的试剂瓶充满CO2后,注入同体积的水和NaOH溶液,比较气球胀大的程度等.
分析 根据氢氧化钠可以与二氧化碳反应生成碳酸钠和水,生成的碳酸钠可以与酸反应生成二氧化碳气体,也可以与含钙离子或钡离子的物质结合产生沉淀进行分析.
解答 解:(1)氢氧化钠可以与二氧化碳反应生成碳酸钠和水,气体被消耗,导致瓶内压强减小,在大气压的作用下,气球鼓起,化学方程式为:CO2+2NaOH=Na2CO3+H2O;
(2)氢氧化钠和二氧化碳生成的碳酸钠可以与酸反应生成二氧化碳气体,也可以与含钙离子或钡离子的物质结合产生沉淀,要证明二者发生了化学反应,只需证明生成了碳酸钠即可,需要做的实验为:在反应后的溶液中滴入Ba(OH)2溶液(或Ca(OH)2溶液);或在反应后的溶液中滴入稀盐酸;或取两个同样的试剂瓶充满CO2后,注入同体积的水和NaOH溶液,比较气球胀大的程度等.
故答案为:(1)气球胀大,CO2和NaOH反应使瓶内气压减小,CO2+2NaOH=Na2CO3+H2O;
(2)在反应后的溶液中滴入Ba(OH)2溶液(或Ca(OH)2溶液);或在反应后的溶液中滴入稀盐酸;或取两个同样的试剂瓶充满CO2后,注入同体积的水和NaOH溶液,比较气球胀大的程度等.
点评 本题考查了氢氧化钠与二氧化碳的反应以及碳酸盐的检验,完成此题,可以依据已有的知识进行.所以要求同学们在品是的学习中加强基础知识的储备,以便能够灵活应用.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
7. 根据下列溶解度表和溶解度曲线图回答问题.
根据下列溶解度表和溶解度曲线图回答问题.
(1)图中硝酸钾的溶解度曲线是甲.
(2)50℃时,乙的溶解度为是40g.
(3)60℃时,将甲、乙、丙的固体各40g分别加入100g水中充分溶解后,能形成饱和溶液的是丙.
(4)要使接近饱和的甲物质溶液变为饱和溶液,可采取的一种措施是降低温度.
 根据下列溶解度表和溶解度曲线图回答问题.
根据下列溶解度表和溶解度曲线图回答问题.| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| KNO3的溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)50℃时,乙的溶解度为是40g.
(3)60℃时,将甲、乙、丙的固体各40g分别加入100g水中充分溶解后,能形成饱和溶液的是丙.
(4)要使接近饱和的甲物质溶液变为饱和溶液,可采取的一种措施是降低温度.
8.下列关于水的叙述正确的是( )
| A. | 水是由氢气分子和氧气分子组成 | B. | 电解水是将化学能转化为电能 | ||
| C. | 煮沸可以使大多数硬水软化 | D. | 明矾可用于吸附水中的色素和异味 |
5. 如图所示,试管中盛满了氢氧化钠溶液,用导管往试管中缓缓通入二氧化碳和氧气的混合气体.
如图所示,试管中盛满了氢氧化钠溶液,用导管往试管中缓缓通入二氧化碳和氧气的混合气体.
(1)试管中最后收集到的气体是氧气;
(2)试管内发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
 如图所示,试管中盛满了氢氧化钠溶液,用导管往试管中缓缓通入二氧化碳和氧气的混合气体.
如图所示,试管中盛满了氢氧化钠溶液,用导管往试管中缓缓通入二氧化碳和氧气的混合气体.(1)试管中最后收集到的气体是氧气;
(2)试管内发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.
9.在氯化钡溶液中滴入某种溶液,生成白色沉淀,则有关说法错误的是( )
| A. | 该反应不是复分解反应 | B. | 反应后溶液可能呈酸性 | ||
| C. | 白色沉淀可能溶于盐酸 | D. | 滴入的可能是硝酸银溶液 |
7. 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的 Zn粉,溶液质量随反应时间变化的情况如图所示.下列说法不正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的 Zn粉,溶液质量随反应时间变化的情况如图所示.下列说法不正确的是( )
 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的 Zn粉,溶液质量随反应时间变化的情况如图所示.下列说法不正确的是( )
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的 Zn粉,溶液质量随反应时间变化的情况如图所示.下列说法不正确的是( )| A. | 取a点溶液,滴加稀盐酸,有白色沉淀产生 | |
| B. | 图标上b→c段溶液质量增加的原因是Zn与Cu(NO3)2溶液反应 | |
| C. | b点时溶液中金属离子有Zn2+、Cu2+,容器底部金属单质有Zn、Cu、Ag | |
| D. | c点和d点溶液中溶质种类相同,容器底部金属种类也相同 |