题目内容
1.用10克石灰石与足量稀盐酸反应,生成3.3克二氧化碳,求石灰石中碳酸钙的百分含量.分析 根据题干提供的数据结合碳酸钙和稀盐酸反应的化学方程式进行分析解答即可.
解答 解:设碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{44}=\frac{x}{3.3g}$
x=7.5g
碳酸钙的百分含量为:$\frac{7.5g}{10g}×100%$=75%
答:石灰石中碳酸钙的百分含量为75%.
点评 本题考查的是根据化学方程式的计算,完成此题的关键是写对化学方程式,掌握根据化学方程式计算的一般步骤.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.点燃蜡烛,在蜡烛火焰上方罩一个干净的冷烧杯,过一段时间后,取下烧杯,往烧杯中加入澄清石灰水,振荡.下列有关实验现象描述错误的是( )
| A. | 生成水和二氧化碳 | B. | 澄清石灰水变浑浊 | ||
| C. | 蜡烛的火焰分为三层 | D. | 罩在火焰上的烧杯内壁出现水珠 |
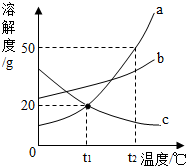 如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题:
如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题: