题目内容
6.有关水的实验装置如图所示.
(1)图甲为简易净水装置,其中活性炭的作用是吸附;图乙为蒸馏装置,海水依次经图甲与图乙装置处理后,所得的水是软水(填“硬水”或“软水”).
(2)图丙为简易水电解器,电解水的化学符号表达式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,B管中产生的气体是氢气.
(3)如果要检验自来水是否为软水,只需在试管中取样,加入适量肥皂水,震荡后观察到有较多的泡沫,则证明自来水为软水.
分析 (1)根据活性炭具有吸附性以及蒸馏得到的水为纯净物进行解答;
(2)根据水通电分解产生氢气和氧气,正极氧气,负极产生氢气分析;
(3)根据硬水和软水的鉴别方法分析.
解答 解:(1)活性炭具有吸附性,除去水中的异味;蒸馏水中几乎不含有杂质,属于软水;
(2)水通电分解产生氢气和氧气,正极氧气,负极产生氢气,所以电解水的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;B管中产生的气体是电源的负极产生的气体,较多是氢气;
(3)如果要检验自来水是否为软水,只需在试管中取样加入适量肥皂水,振荡后观察到产生泡沫多,则证明自来水为软水.
答案:
(1)吸附;软水;
(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢气;
(3)有较多的泡沫.
点评 本题考查知识难度不大,但涉及面较广,很好的体现了化学知识与生活的联系,提醒同学们在学习知识的同时,要注意联系实际,灵活分析解答问题.

练习册系列答案
相关题目
16.普通蜡烛容易熄灭,有人对此做出改进,研究出一种“吹不灭”的蜡烛.吹灭蜡烛后,蜡烛总能灭而复燃.同学们对此进行了探究.
【初步探究】为何这种蜡烛总能灭而复燃?
【查阅资料】①这种蜡烛芯里包裹一层打火石粉末.打火石是由镁、铝、铁中的一种或二种金属掺入少量稀土元素制成的合金,它的着火点为150℃.当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃.
②镁、铝、铁三种金属中,只有铝能和NaOH溶液反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑
【反思一】这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?金属不与氧气(空气)接触,如要熄灭这种蜡烛,可采用的方法是隔绝氧气或剪除灯芯或用湿抹布盖灭等.
【深入探究】打火石中的金属主要是什么成分?
同学们进行了如下探究:(注:不考虑打火石中稀土元素对探究金属性质的影响)
表格中的实验现象依次是:溶液为无色(或溶液不呈浅绿色),有大量气泡产生,固体部分溶解.
【反思二】甲同学提出:在实验步骤1时,可直接观察“金属产生气泡的快慢”这一现象来判断该金属.老师否定了这一方案,理由是未知金属只有一种,没有参照金属对比,无法判断金属的种类(或无法判断反应速率的快慢;或该金属是混合物无法判断速度).
【初步探究】为何这种蜡烛总能灭而复燃?
【查阅资料】①这种蜡烛芯里包裹一层打火石粉末.打火石是由镁、铝、铁中的一种或二种金属掺入少量稀土元素制成的合金,它的着火点为150℃.当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃.
②镁、铝、铁三种金属中,只有铝能和NaOH溶液反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑
【反思一】这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?金属不与氧气(空气)接触,如要熄灭这种蜡烛,可采用的方法是隔绝氧气或剪除灯芯或用湿抹布盖灭等.
【深入探究】打火石中的金属主要是什么成分?
同学们进行了如下探究:(注:不考虑打火石中稀土元素对探究金属性质的影响)
| 实验步骤 | 实验现象 | 实验结论 |
| 1取样,加入足量的稀盐酸 | 有大量气泡产生,固体全部溶解, | 打火石中不含铁 |
| 2另取样,加入足量的NaOH溶液 | 有大量气泡产生,固体部分溶解 | 打火石中含有镁、铝 |
【反思二】甲同学提出:在实验步骤1时,可直接观察“金属产生气泡的快慢”这一现象来判断该金属.老师否定了这一方案,理由是未知金属只有一种,没有参照金属对比,无法判断金属的种类(或无法判断反应速率的快慢;或该金属是混合物无法判断速度).
11.4g碳和10g的氧气充分反应并只生成二氧化碳,则二氧化碳的质量是( )
| A. | 14.7g | B. | 13.75g | C. | 14g | D. | 无法确定 |
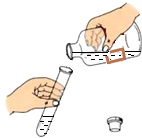 图为液体药品取用的示意图,仔细观察,指出操作中的错误.
图为液体药品取用的示意图,仔细观察,指出操作中的错误.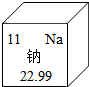 在元素周期表中,钠元素的信息如图所示.钠属于金属(填“金属”或“非金属”)元素,其中一个原子中质子数为11,钠离子的结构示意图为
在元素周期表中,钠元素的信息如图所示.钠属于金属(填“金属”或“非金属”)元素,其中一个原子中质子数为11,钠离子的结构示意图为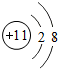 ,金属钠易与空气中的氧气反应生成氧化钠,反应方程式为4Na+O2═2Na2O.
,金属钠易与空气中的氧气反应生成氧化钠,反应方程式为4Na+O2═2Na2O.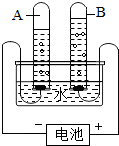 图为水通电分解的实验装置图,据图分析:
图为水通电分解的实验装置图,据图分析: