题目内容
17.生活离不开化学(1)多吃蔬菜、水果补充人体所需要的维生素.
(2)区分硬水和软水的方法是加入肥皂水.
(3)纸箱着火了,用水浇灭的原理是使可燃物的温度降低到着火点以下.
(4)将生锈的铁钉投入到稀硫酸中,观察到的现象是铁锈逐渐溶解,溶液变黄,化学反应方程式是Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
分析 (1)根据蔬菜中富含的营养素来分析;
(2)根据已有的硬水和软水的鉴别方法进行分析解答即可;
(3)根据灭火的原理来分析;
(4)铁锈的主要成分是氧化铁,把生锈的铁钉放到足量的稀硫酸中,表面的铁锈先与硫酸反应,据此写出反应的化学方程式即可.
解答 解:(1)蔬菜、水果中富含维生素,所以多吃蔬菜、水果补充人体所需要的维生素;故填:维生素;
(2)鉴别硬水和软水使用的是肥皂水,硬水与肥皂水混合有浮渣产生,而软水与肥皂水混合有泡沫产生,故填:肥皂水;
(3)水灭火,水蒸发时吸收热量,可使温度降低到可燃物的着火点以下,从而达到灭火的目的;故填:使可燃物的温度降低到着火点以下;
(4)铁锈的主要成分是氧化铁,生锈的铁钉放入稀硫酸中,铁锈的主要成分氧化铁与稀硫酸反应生成硫酸铁和水,会观察到铁锈逐渐溶解,溶液变黄;反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;故填:铁锈逐渐溶解,溶液变黄;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
点评 本题考查了营养素的来源、硬水与软水的鉴别方法、灭火的原理、酸的化学性质以及化学方程式的书写,难度不大.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
7.如图分别与相应的操作过程相对应,其中正确的是( )
| A. | 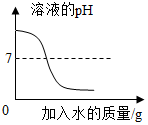 向pH=10的氢氧化钙溶液中不断加水稀释 | |
| B. | 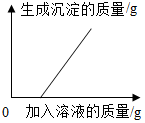 向含有硫酸的硫酸铜溶液中加入过量的氢氧化钠溶液 | |
| C. | 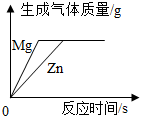 向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片 | |
| D. |  向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化) |
12.下列实验方案能达到目的是( )
| A. | 证明某气体是一氧化碳,将该气体通过灼热的氧化铜,黑色粉末变红 | |
| B. | 证明酸碱恰好完全反应,向含有酚酞的氢氧化钠溶液中加入盐酸,溶液最终呈无色 | |
| C. | 证明燃烧条件之一温度达到着火点,用玻璃棒分别蘸取酒精和水,放在酒精灯上加热 | |
| D. | 证明铁、锌、铜金属的活动性顺序,分别将铁片、锌片、铜片放入等体积等浓度的稀硫酸中 |
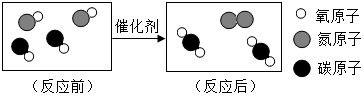
2.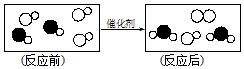 如图是将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法的正确的是( )
如图是将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法的正确的是( )
 如图是将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法的正确的是( )
如图是将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法的正确的是( )| A. | 该反应是置换反应 | |
| B. | 该反应中元素的化合价均未发生改变 | |
| C. | 参加反应的两种分子的个数比为1:1 | |
| D. | 化学反应有三种新物质生成 |
7.兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究.
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
查阅资料:
【得出结论1】三种溶液的碱性由强到弱的顺序为氢氧化钠溶液>碳酸钠溶液>碳酸氢钠溶液.
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由无色变为红色.向其中加入稀盐酸,该反应的化学方程式为NaOH+HCl=NaCl+H2O.
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图1所示.
【得出结论2】从微观角度分析,该反应的实质是氢离子和氢氧根离子结合生成水分子.
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得列pH变化与时间的关系如图2、图3所示.
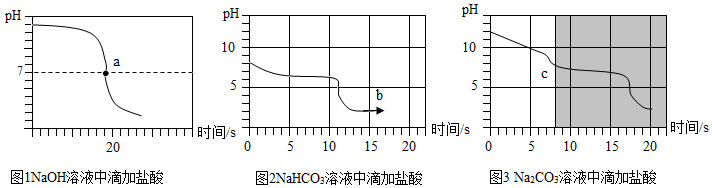
【交流与反思】b点的溶质为NaCl、HCl(写化学式),将图2和图3的阴影部分进行叠加,发现两者基本重合,c点的溶质NaCl、NaHCO3(写化学式)
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示:Na2CO3+HCl=NaCl+NaHCO3、NaHCO3+HCl═NaCl+H2O+CO2↑.
【结论与反思】探究溶液的酸碱性及反应pH值的变化,可以认识反应的原理及进行的过程.
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
| 液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
| 紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
| pH | 7.5~9 | 10~11.9 | 12~14 |
| 紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由无色变为红色.向其中加入稀盐酸,该反应的化学方程式为NaOH+HCl=NaCl+H2O.
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图1所示.
【得出结论2】从微观角度分析,该反应的实质是氢离子和氢氧根离子结合生成水分子.
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得列pH变化与时间的关系如图2、图3所示.

【交流与反思】b点的溶质为NaCl、HCl(写化学式),将图2和图3的阴影部分进行叠加,发现两者基本重合,c点的溶质NaCl、NaHCO3(写化学式)
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示:Na2CO3+HCl=NaCl+NaHCO3、NaHCO3+HCl═NaCl+H2O+CO2↑.
【结论与反思】探究溶液的酸碱性及反应pH值的变化,可以认识反应的原理及进行的过程.
 如图是某反应的微观示意图.
如图是某反应的微观示意图.
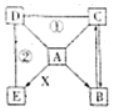 已知A、B、C、D是不同类别的物质,反应①有白色沉淀生成,反应②有红褐色沉淀生成.X是赤铁矿的主要成分.(图中“→”表示物质间存在转化关系.“--”表示两种物质间能发生反应
已知A、B、C、D是不同类别的物质,反应①有白色沉淀生成,反应②有红褐色沉淀生成.X是赤铁矿的主要成分.(图中“→”表示物质间存在转化关系.“--”表示两种物质间能发生反应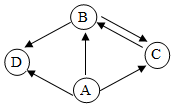 如图A,B,C,D是初中化学中常见的四种物质,其中A为黑色单质,D为红色单质,B、C是组成元素相同的两种气态化合物.“→”表示物质间的转化关系(部分反应物、生成物及反应条件乙省略).请回答:
如图A,B,C,D是初中化学中常见的四种物质,其中A为黑色单质,D为红色单质,B、C是组成元素相同的两种气态化合物.“→”表示物质间的转化关系(部分反应物、生成物及反应条件乙省略).请回答: