题目内容
配制100g溶质的质量分数为8%的氢氧化钠溶液,需要氢氧化钠和水各多少克?若要完全中和这些溶液,需要溶质的质量分数为9.8%的稀硫酸多少克?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:有关化学方程式的计算
分析:已知溶液质量、溶质质量分数,可以计算溶质、溶剂的质量;
氢氧化钠和稀硫酸反应生成硫酸钠和水,根据氢氧化钠的质量可以计算硫酸的质量,进一步可以计算稀硫酸的质量.
氢氧化钠和稀硫酸反应生成硫酸钠和水,根据氢氧化钠的质量可以计算硫酸的质量,进一步可以计算稀硫酸的质量.
解答:解:配制100g溶质的质量分数为8%的氢氧化钠溶液,需要氢氧化钠的质量为:100g×8%=8g,需要水的质量为:100g-8g=92g,
设要完全中和这些溶液,需要溶质的质量分数为9.8%的稀硫酸的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
8g x×9.8%
=
,
x=100g,
答:配制100g溶质的质量分数为8%的氢氧化钠溶液,需要氢氧化钠和水的质量分别是8g、92g,若要完全中和这些溶液,需要溶质的质量分数为9.8%的稀硫酸100g.
设要完全中和这些溶液,需要溶质的质量分数为9.8%的稀硫酸的质量为x,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
8g x×9.8%
| 80 |
| 98 |
| 8g |
| x×9.8% |
x=100g,
答:配制100g溶质的质量分数为8%的氢氧化钠溶液,需要氢氧化钠和水的质量分别是8g、92g,若要完全中和这些溶液,需要溶质的质量分数为9.8%的稀硫酸100g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便.下列各组物质中,符合“氧化物-酸-碱-盐”顺序排列的是( )
| A、HClO HCl Mg(OH)2 MgCl2 |
| B、CO2 H2CO3 CaCO3 Ca(HCO3)2 |
| C、SO3 NaHSO4 NaOH Na2SO4 |
| D、H2O CH3COOH NH3?H2O NH4Cl |
知识梳理有助于我们对已学知识进行巩固,如图是某同学学习物质构成的奥秘后以氧气为例进行的梳理;下列选项中与a、c相对应的是( )


| A、原子核、核外电子 |
| B、原子、核外电子 |
| C、原子、原子核 |
| D、核外电子、原子 |
 亮亮同学对课本上的有关实验(如图)有几个疑问.请你发挥自己的聪明才智为他解答以下问题:
亮亮同学对课本上的有关实验(如图)有几个疑问.请你发挥自己的聪明才智为他解答以下问题:

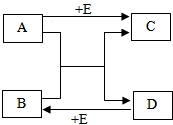 已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如下图所示.如果已知A和B均为黑色固体,C是造成温室效应的主要气体,D是一种亮红色的金属单质.则回答:
已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如下图所示.如果已知A和B均为黑色固体,C是造成温室效应的主要气体,D是一种亮红色的金属单质.则回答: