题目内容
11.同学们欲测定某石灰石样品中碳酸钙的质量分数:取该石灰石样品40g,把120g稀盐酸分三次加入,实验过程所得数据如下表(已知石灰石样品中的杂质不溶于水,不与稀盐酸反应):| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 40 | 30 |
| 2 | 40 | 20 |
| 3 | 40 | 13.6 |
(2)求所用盐酸中溶质的质量分数.
分析 (1)根据表中的数据可知,每40g稀盐酸反应的碳酸钙的质量是40g-30g=10g,在第三次加入的40g的稀盐酸反应的碳酸钙的质量是20g-13.6g=6.4g,说明了盐酸有剩余,13.6g的 剩余固体是杂质,据此可计算出碳酸的质量分数;
(2)根据10g碳酸钙的质量可求出40g的稀盐酸中溶质的质量,再根据溶质的质量分数的计算公式计算出盐酸中溶质的质量分数.
解答 解:(1)由1、2次实验可知,40g稀盐酸恰好和10g碳酸钙反应,第3次时盐酸有剩余,剩余的固体是杂质,样品中碳酸钙的质量分数:$\frac{40g=13.6g}{40g}×100%$=66%
(2)设40g稀盐酸中氯化氢质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73
10g x
$\frac{100}{73}=\frac{10g}{x}$ 解得:x=7.3g
稀盐酸中溶质的质量分数为:$\frac{7.3g}{40g}×100%$=18.25%,
故答为:(1)66%;(2)所用盐酸中溶质的质量分数18.25%.
点评 本题主要考查学生根据化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.下列结构示意图中的粒子,化学性质相似的是( )
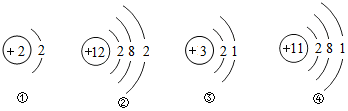

| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
6.除去下列物质中含有的少量杂质(括号内的物质),所选试剂不合理的是( )
| A. | NaOH溶液 (Na2CO3):过量的Ca(OH)2溶液 | |
| B. | CaCl2溶液(HCl):过量的CaCO3 | |
| C. | Cu粉(Fe):足量的稀硫酸 | |
| D. | CO(CO2):足量的氢氧化钠溶液 |
16.青少年正处于长身体的重要阶段,一定要每天摄入适量的蛋白质,下列物质富含蛋白质的物质是( )
| A. | 荔枝 | B. | 芸豆 | C. | 大米饭 | D. | 黄豆 |
20.下列有关化学实验的“目的→操作→现象→结论”的描述都正确的是( )
| 选项 | 目的 | 操作 | 现象 | 结论 |
| A | 检验集气瓶中是否集满二氧化碳 | 将燃着的木条伸入集气瓶中 | 燃着的木条熄灭 | 集气瓶中已集满二氧化碳 |
| B | 比较人体吸入的空气和呼出的气体中氧气的含量 | 分别向盛有空气和呼出气体的集气瓶中伸入燃着的木条 | 燃着的木条在空气中继续燃烧,在呼出气体中熄灭 | 空气中的氧气含量高于呼出气体 |
| C | 比较铝和铜的金属活动性 | 将砂纸打磨过的铝丝浸入到硫酸铜溶液中 | 铝丝表面有红色铜析出 | 铝比铜活泼 |
| D | 证明久置空气中的烧碱溶液是否变质 | 取样后滴加无色酚酞试液 | 溶液变红 | 烧碱溶液变质 |
| A. | A | B. | B | C. | C | D. | D |
18.二茂铁甲酸(化学式:C11H20FeO2)是一种光敏剂,可用于不对称有机合成催化剂,燃烧控制剂或调节剂,在高分子材料中也可作催化剂和改良剂.下列有关二茂铁甲酸说明不正确的是( )
| A. | 每个二茂铁甲酸分子中含有24个原子 | |
| B. | 该物质有四种元素组成 | |
| C. | 该物质中氧元素质量分数最小 | |
| D. | 该物质中碳、氢元素的质量比为66:5 |