题目内容
15.化学活动小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓硫酸能否发生反应呢?[猜想与假设]
猜想1:在常温下能反应;
猜想2:在常温下不能反应,但在加热条件下能反应;
猜想3:在加热条件下也不能反应.
[实验与事实]
操作1:将一小块铜片放入试管中,加入足量的浓硫酸,无明显现象;
操作2:加热该试管,铜片上有气泡生成,并闻到刺激性气味;
操作3:检验产生的有刺激性气味的气体(检验方法及现象略);
操作4:立即停止加热;
操作5:将少量水慢慢倒入试管中的残液中,发现有少量液滴飞溅,溶液呈蓝色.
[结论与解释]
(1)由以上探究可知猜想②正确的.(填序号)
(2)经检验产生的气体是SO2,立即停止加热是为了避免产生更多的SO2;
(3)铜跟浓硫酸在加热条件下反应的产物是SO2和CuSO4.
[反思与评价]
(1)从安全角度考虑,对操作5作出评价从安全角度考虑不能将水倒入剩余的液体里,理由是如果浓硫酸有剩余,溶于水放热,比较危险;
(2)请你对“结论与解释”(3)合理性作出评价不正确;反应物中有氢元素,但二氧化硫和硫酸铜中都不含氢元素.
[拓展与应用]根据以上探究和已掌握的知识,同学们又设计了两个利用废铜屑、硫酸为原料制取硫酸铜的实验方案.
甲方案:利用废铜屑和浓硫酸在加热的条件下反应制取CuSO4
乙方案:在加热条件下将废铜屑在空气中氧化成CuO,再将CuO与稀硫酸反应制取CuSO4.
请你从安全、环保等方面对较差的方案作出评价:甲的方案比较差;利用废铜屑和浓硫酸在加热的条件下反应制取CuSO4,浓硫酸具有极强的腐蚀性,使用不安全,有一部分硫元素转化成二氧化硫,污染空气,且造成原料的浪费.
分析 结论与解释:从实验的过程可以证明铜和浓硫酸能反应,生成物中有二氧化硫和硫酸铜,其中的二氧化硫是有毒气体,不能直接排放到空气中,应该用碱液吸收.
反思与评价:浓硫酸溶于水要放出大量的热,所以浓硫酸不能倒入水中,浓硫酸中含有氢元素,生成物中也要有氢元素;
拓展与运用:考虑制取硫酸铜的方案的优缺点时,要从原料的利用率,环保,安全等方面考虑.
解答 解:[结论与解释](1)根据实验操作和现象,可以证明铜和浓硫酸在加热的时候能反应,生成物中有二氧化硫和硫酸铜,所以猜想②正确;
[反思与评价]:
(3)操作5中,从安全角度考虑不能将水倒入剩余的液体里,理由是如果浓硫酸有剩余,溶于水放热,比较危险;
浓硫酸溶于水会放出大量的热,造成液滴飞溅,所以不能把含浓硫酸的物质倒入水中.
(4)因为反应物中有氢,硫、氧、铜四种元素,根据反应前后元素的种类不变的原则,生成物中应该有氢元素,所以生成物质中除二氧化硫和硫酸铜外还有含有氢元素的物质存在.
[拓展与运用]
(5)比较这两个方案,从经济,环保,安全的角度考虑,浓硫酸使用时要注意安全,二氧化硫有毒等,通过综合考虑,利用废铜屑和浓硫酸在加热的条件下反应制取CuSO4,浓硫酸具有极强的腐蚀性,使用不安全,有一部分硫元素转化成二氧化硫,污染空气,且造成原料的浪费,CuO与稀硫酸反应直接生成硫酸铜和水,所以方案乙比甲要好的多;
故答案为:
(1)②;
(3)从安全角度考虑不能将水倒入剩余的液体里,理由是如果浓硫酸有剩余,溶于水放热,比较危险;
(4)不正确;反应物中有氢元素,但二氧化硫和硫酸铜中都不含氢元素;
(5)甲的方案比较差,利用废铜屑和浓硫酸在加热的条件下反应制取CuSO4,浓硫酸具有极强的腐蚀性,使用不安全,有一部分硫元素转化成二氧化硫,污染空气,且造成原料的浪费;
点评 本题属于实验设计题,排在氢后的金属不与酸发生置换反应,但是可以和强氧化性的酸反应,浓硫酸具有强氧化性,完成本题,可以从题干给出的内容,提取有用的信息,分析归纳从而得出合理的答案,本考点主要出现在实验题中.

 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案| A. | NaOH | B. | H2SO4 | C. | HCl | D. | Na2CO3 |
| A. | 铜用于制导线,是由于铜有良好的导电性 | |
| B. | 氮气常用作保护气,是由于氮气的化学性质不活泼 | |
| C. | 酒精做燃料,是由于酒精具有可燃性 | |
| D. | 氧气用于切割、气焊,是由于氧气具有可燃性 |
【提出问题】氢氧化钠溶液是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
| 实 验 步 骤 | 实 验 现 象 | 结 论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | 有白色沉淀产生 | 说明氢氧化钠溶液已经变质 |
(2)小李同学认为小王同学的结论不科学,其理由是:碳酸钠溶液显碱性,溶液的pH>7.
(3)小李同学的实验中观察到实验现象A为:有白色沉淀产生.
(4)小张同学认为该氢氧化钠溶液只是部分变质.为确定小张同学的猜想,应该对小李同学的实验进行如下改进:向试管中加入过量的氯化钡溶液,再向试管中滴加酚酞溶液,通过观察溶液颜色变化来检验该溶液是否含有氢氧化钠.如果只是部分变质,观察到的现象是:先有白色沉淀产生,后来酚酞变成红色.
(5)若要除去上述变质的氢氧化钠溶液中的杂质应加入适量的Ca(OH)2(填化学式)溶液而除去.
 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 连电源负极的管(A)中气体 | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 |
| 连电源正极的管(B)中气体 | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 |
(2)装置气密性良好、读数正确,但电解开始阶段两管气体的体积比不符合理论比值的原因是氧气的溶解性大于氢气的溶解性.
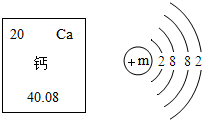 如图是钙在元素周期表中的相关信息及钙原子结构示意图,下列说法中错误的是( )
如图是钙在元素周期表中的相关信息及钙原子结构示意图,下列说法中错误的是( )| A. | m的数值是20 | B. | 钙属于金属元素 | ||
| C. | 钙元素在化合物中显+2价 | D. | 钙元素的质量是40.08g |
| A. | 氧气 | B. | 氮气 | C. | 稀有气体 | D. | 二氧化碳 |
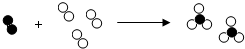 在实验室中,取140克化合物甲与30克化合物乙完全反应恰好生成170克的化合物丙.其反应的微观示意图如下,甲表示为
在实验室中,取140克化合物甲与30克化合物乙完全反应恰好生成170克的化合物丙.其反应的微观示意图如下,甲表示为 ,乙表示为
,乙表示为 ,丙表示为
,丙表示为 .
.