题目内容
将10g碳酸钙固体高温煅烧一段时间,冷却后投入足量稀盐酸中完全反应,有关结论错误的是( )
|
| A. | 共生成0.1mol氯化钙 |
|
| B. | 燃烧越充分则消耗的盐酸越少 |
|
| C. | 共生成0.1mol二氧化碳 |
|
| D. | 燃烧后固体中氧元素的质量分数减小 |
考点:
盐的化学性质;元素的质量分数计算;根据化学反应方程式的计算.
专题:
常见的盐 化学肥料.
分析:
A、根据10g碳酸钙的物质的量是0.1mol,结合钙元素守恒,生成的氧化钙也是0.1mol进行分析;
B、根据碳酸钙、氧化钙和盐酸都会生成氯化钙,然后结合钙元素守恒进行解答;
C、根据碳酸钙高温生成氧化钙和二氧化碳进行分析;
D、根据反应前固体是碳酸钙,反应后的固体是氧化钙进行分析.
解答:
解: =0.1mol,
=0.1mol,
A、10g碳酸钙的物质的量是0.1mol,结合钙元素守恒,生成的氧化钙也是0.1mol,故A正确;
B、碳酸钙、氧化钙和盐酸都会生成氯化钙,然后结合钙元素守恒,所以生成的氯化钙也始终是0.1mol,故B错误;
C、CaCO3 CaO+CO2↑,他化学方程式可以看出,生成0.1mol二氧化碳,故C正确;
CaO+CO2↑,他化学方程式可以看出,生成0.1mol二氧化碳,故C正确;
D、反应前固体是碳酸钙,反应后的固体是氧化钙,所以固体中氧元素的质量分数减小,故D正确.
故选:B.
点评:
本题主要考查了物质的量再化学方程式为中的应用,难度不大,需要多加训练.

化学学习中常用到“质量守恒”、“反应先后”等思想来分析、解决问题.下列推断正确的是( )
|
| A. | 50mL酒精中加入50mL水,根据溶质守恒推出酒精溶液的溶质质量分数为50% |
|
| B. | 酒精燃烧生成CO2和H2O的分子个数比为2:3,根据原子守恒推出酒精分子中C、H原子个数比为1:3 |
|
| C. | 少量铁粉放入硝酸银和硝酸铜的混合溶液中,根据反应的先后推出析出固体铜 |
|
| D. | 向硫酸铜与硫酸的混合溶液中滴加氢氧化钠溶液,根据反应的先后推出先生成蓝色沉淀 |
天平两边各放质量相等的烧杯,分别装入等质量,等溶质质量分数的稀硫酸,此时天平平衡,将等质量的MgCO3和Na2CO3分别加入两烧杯中,充分反应后,下列说法错误的是( )
|
| A. | 若天平不平衡,指针一定偏向加Na2CO3的一边 |
|
| B. | 若天平平衡,两烧杯中的酸一定完全反应 |
|
| C. | 若反应后Na2CO3有剩余,天平一定平衡 |
|
| D. | 若天平不平衡,两种碳酸盐一定都没有剩余 |
化学与日常生活、工农业生产密切相关.下列说法中不正确的是( )
|
| A. | 用含有碳酸氢钠的发酵粉焙制糕点 |
|
| B. | 工业上用熟石灰处理硫酸厂的污水 |
|
| C. | 医疗上用纯酒精作消毒剂 |
|
| D. | 生活中用含有NaOH的清洁剂去油污 |
下列实验中利用提供的方案不能达到目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 稀释浓硫酸 | 将浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
| B | 鉴别氮气和氧气 | 将带火星的木条插入集气瓶中,看是否复燃 |
| C | 测某溶液的酸碱度 | 滴入酚酞试液,观察溶液颜色的变化 |
| D | 除去固体氯化钾中少量的二氧化锰 | 加水溶解后,过滤、蒸发 |
|
| A. | A | B. | B | C. | C | D. | D |
 、
、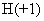 、
、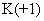 、
、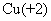 、
、 ,请选择元素,写出符合要求的化合物的化学式:
,请选择元素,写出符合要求的化合物的化学式: