题目内容
18.判断金属铝比铁更活泼的依据是( )| A. | 相同条件下跟酸溶液反应生成氢气的质量,铝比铁多 | |
| B. | 相同条件下跟酸溶液反应,铝的反应速度比铁快 | |
| C. | 铁能把铝从氯化铝溶液中置换出来 | |
| D. | 相同条件下,铝、铁都能将硫酸铜溶液中的铜置换出来 |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,且金属的活动性越强,反应越剧烈;位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此结合事实进行分析判断.
解答 解:A、相同条件下跟酸溶液反应生成氢气的质量,铝比铁多,不能判断金属铝比铁更活泼,故选项错误.
B、相同条件下跟酸溶液反应,铝的反应速度比铁快,能判断金属铝比铁更活泼,故选项正确.
C、铁不能把铝从氯化铝溶液中置换出来,故选项错误.
D、相同条件下,铝、铁都能将硫酸铜溶液中的铜置换出来,只能说明铁、铝比铜活泼,不能判断铁、铝的活动性强弱,故选项错误.
故选B.
点评 本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
8.下列变化中,氧元素由化合态变为游离态的是( )
| A. | 水通电生成氢气和氧气 | B. | 氢气和氧气反应生成水 | ||
| C. | 水和生石灰反应生成熟石灰 | D. | 从空气中分离出氧气 |
9.如图所示的四个图象,能正确反映对应变化关系的是( )
| A. | 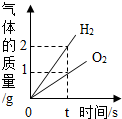 水的电解 | B. | 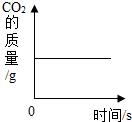 木炭在密闭容器中燃烧 | ||
| C. | 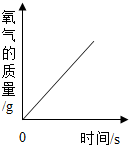 加热一定量的高锰酸钾制氧气 | D. | 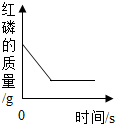 过量红磷测定空气中氧气含量 |
6. 碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.
碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.
【查阅资料】
Ⅰ.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
Ⅱ.碳酸钠溶液呈碱性.
【进行实验】为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠(或水雾等).
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3.
①他们的依据是量守恒定律(或化学反应前后元素种类不变或化学反应前后原子种类不变或NaHCO3中含有Na、H、C、O元素).
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写如表:
【讨论与评价】实验一的结论与实验二、实验三的结论相反,在讨论时兴趣小组的同学认为方案一的结论不正确,他们的理由是碳酸钠溶液呈碱性,也能使无色酚酞变成红色.
【总结】请写出碳酸氢钠受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(4)某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质),取样品10.0g逐滴加入稀盐酸,所得气体的质量为4.4g.
求:样品中碳酸氢钠的质量分数.
 碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.
碳酸氢钠常用于食品和医药工业,某化学兴趣小组对碳酸氢钠进行探究.【查阅资料】
Ⅰ.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质.
Ⅱ.碳酸钠溶液呈碱性.
【进行实验】为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠(或水雾等).
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3.
①他们的依据是量守恒定律(或化学反应前后元素种类不变或化学反应前后原子种类不变或NaHCO3中含有Na、H、C、O元素).
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写如表:
| 实验 | 实验现象 | 结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 | 溶液变成红色 | 固体产物是NaOH, 而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入氯化钙溶液 | 产生白色沉淀 | 固体产物是Na2CO3, 而不是NaOH |
| 实验三:取少量反应后的固体产物,加入过量稀盐酸(或稀硫酸、稀硝酸、醋酸) | 产生大量气泡 | 固体产物是Na2CO3, 而不是NaOH |
【总结】请写出碳酸氢钠受热分解的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(4)某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质),取样品10.0g逐滴加入稀盐酸,所得气体的质量为4.4g.
求:样品中碳酸氢钠的质量分数.
3.在一定条件下,甲乙丙丁四种物质在一密闭容器内充分反应.测得反应前后各物质的质量如下表所示,回答以下问题:
(1)m的值为1;该反应的基本类型是化合反应
(2)参加反应的乙、丁的质量比是3:2
(3)若乙、丙的摩尔质量之比为3:2,则两者的化学计量数之比为2:5.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 1 | 20 | 15 | 8 |
| 反应后质量/g | m | 11 | 30 | 2 |
(2)参加反应的乙、丁的质量比是3:2
(3)若乙、丙的摩尔质量之比为3:2,则两者的化学计量数之比为2:5.
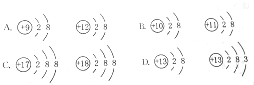 分析下列各组粒子的结构示意图,仿照示例,说出其余三组表示的意义.
分析下列各组粒子的结构示意图,仿照示例,说出其余三组表示的意义. A、B、C、D是初中化学常见的物质,这四种物质均含有同一种元素,其中A为无色气体单质,B、C为氧化物且B为有毒气体,D是大理石的主要成分.它们之间的部分转化关系如图所示(图中反应条件及部分反应物、生成物已省略)
A、B、C、D是初中化学常见的物质,这四种物质均含有同一种元素,其中A为无色气体单质,B、C为氧化物且B为有毒气体,D是大理石的主要成分.它们之间的部分转化关系如图所示(图中反应条件及部分反应物、生成物已省略) 已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如下转化关系.
已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如下转化关系.