题目内容
5.区别H2和CO,可用的方法是( )①点燃后观察火焰的颜色 ②点燃后,在火焰上方罩一个冷而干燥的烧杯
③将燃烧产物通入石灰水中 ④与灼热氧化铜反应.
| A. | ①②③④ | B. | ②③ | C. | ③④ | D. | ②③④ |
分析 氢气和一氧化碳都是无色无味的气体,不溶于水,都能燃烧,发出淡蓝色火焰,都具有还原性,能还原氧化铜,但燃烧后生成物不同,可据此鉴别区分.
解答 解:①点燃两种气体,观察火焰的颜色不能鉴别,因为二者燃烧都发出淡蓝色火焰,此项错误;
②点燃两种气体,在火焰上方罩一个冷而干燥的烧杯,烧杯内壁出现水珠的是氢气,无明显现象的是一氧化碳,能够鉴别,此项正确;
③点燃两种气体,将燃烧产物通入石灰水,能使石灰水变浑浊的是一氧化碳燃烧后的生成物的性质,氢气燃烧生成物不能使石灰水变浑浊,能够鉴别,此项正确;
④氢气和一氧化碳都能和灼热的氧化铜反应,使黑色的氧化铜变红,故不能鉴别,此项错误.
因此是②③方法正确;
故选B.
点评 鉴别物质时要根据物质的性质,通过明显的现象鉴别,氢气和一氧化碳燃烧后的生成物不同,故可根据生成物区分,除了把生成物通入石灰水中外,还可以在火焰上方罩一个干燥的烧杯进行判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HCl+HClO.产物中,次氯酸HClO是一种弱酸.氯气溶于水所得溶液称为氯水.把品红试纸(染有品 红颜料的滤纸)放入氯水中,品红试纸褪色.右图是实验室用二氧化锰与浓盐酸在加热条件下制取氯气的成套装置图,请填空:
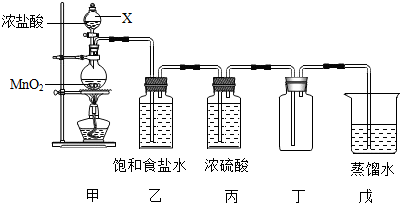
(1)仪器X的名称是:分液漏斗.
(2)装置乙中饱和食盐水的作用是吸收HCl和HClO.
(3)氯气在装置丁中被收集,其收集方法为向上排空气法,装置戊中可得到氯水.
(4)晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】
猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;
猜想4:氯水中的HClO(填化学式)使 品红试纸褪色.
【实验探究】
【结论】学习小组通过讨论,找到了氯水中使品红试纸褪色的物质.
【反思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是氯水先变红后褪色.将氯气通入澄清石灰水中发生反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;2HClO+Ca(OH)2=Ca(ClO)2+2H2O.

(1)仪器X的名称是:分液漏斗.
(2)装置乙中饱和食盐水的作用是吸收HCl和HClO.
(3)氯气在装置丁中被收集,其收集方法为向上排空气法,装置戊中可得到氯水.
(4)晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
【提出问题】氯水中的什么成分使品红试纸褪色?
【猜想】
猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;
猜想4:氯水中的HClO(填化学式)使 品红试纸褪色.
【实验探究】
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| ①把品红试纸放入水中 | 试纸不褪色 | 猜想1不成立 |
| ②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
| ③把品红试纸放入干燥的盐酸中 | 试纸不褪色 | 猜想3不成立 |
【反思】向氯水中滴加几滴紫色石蕊试液,会观察到的现象是氯水先变红后褪色.将氯气通入澄清石灰水中发生反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;2HClO+Ca(OH)2=Ca(ClO)2+2H2O.
20.反应H2+Cu0═Cu+H20,属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
17.下列物质的分类中,不正确的是( )
| A. | 二氧化硫----酸性氧化物 | B. | 空气-----混合物 | ||
| C. | 硫酸氢钠----酸 | D. | 氢氧化钾------碱 |