题目内容
根据下列11-18号元素的原子结构示意图,回答有关问题:
(1)硅原子质子数为 ,最外层有 个电子.
(2)Mg与上述某元素形成的物质中,原子个数比为1:2,该物质的化学式为 .

(1)硅原子质子数为
(2)Mg与上述某元素形成的物质中,原子个数比为1:2,该物质的化学式为
考点:原子结构示意图与离子结构示意图,化学式的书写及意义
专题:化学用语和质量守恒定律
分析:根据原子结构示意的意义及元素的性质与原子的最外层的电子数之间的关系分析回答.
解答:解:(1)由硅的原子结构示意图不难看出,它的质子数是14,有三个电子层,最外层有4个电子.
(2)由于镁原子的最外层上有2个电子,易失去这两个电子,故镁元素在化合物中一般为+2价,它与某元素形成的物质中原子个数比为1:2,说明另外一种元素应为-1价,即它的原子在化学变化中易得一个电子,由上述原子结构示意图,该原子应为氯原子,最外层有7个电子,易得到1个电子,化合价为-1价,形成的化合物的化学式为:MgCl2.
故答为:(1)14,4;(2)MgCl2.
(2)由于镁原子的最外层上有2个电子,易失去这两个电子,故镁元素在化合物中一般为+2价,它与某元素形成的物质中原子个数比为1:2,说明另外一种元素应为-1价,即它的原子在化学变化中易得一个电子,由上述原子结构示意图,该原子应为氯原子,最外层有7个电子,易得到1个电子,化合价为-1价,形成的化合物的化学式为:MgCl2.
故答为:(1)14,4;(2)MgCl2.
点评:主要考查了原子的结构示意图的意义,培养学生分析信息、解决问题的能力.

练习册系列答案
相关题目
关于催化剂的说法正确的是( )
| A、催化剂只能加快反应速率 |
| B、催化剂在反应前后质量和性质不变 |
| C、不使用催化剂,反应就不能进行 |
| D、催化剂可以改变物质的化学反应速率 |
你认为下列制取氢气的方法中,比较廉价、有可能被推广的是( )
| A、用锌粒和稀盐酸反应制氢气 |
| B、电解水制氢气 |
| C、选用合适的催化剂,利用太阳能分解水制氢气 |
 为测定空气中氧气的含量,小华同学打算设计如图所示的实验方案:在一个隔热效果良好的容器上方安装一个可自由上下移动的活塞(活塞质量忽略不计,起始位置在5刻度处).加热容器,使容器温度达到80℃(已知白磷燃烧所需的最低温
为测定空气中氧气的含量,小华同学打算设计如图所示的实验方案:在一个隔热效果良好的容器上方安装一个可自由上下移动的活塞(活塞质量忽略不计,起始位置在5刻度处).加热容器,使容器温度达到80℃(已知白磷燃烧所需的最低温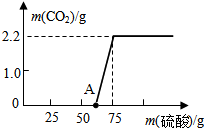 某校研究性学习小组进行了一个有趣的实验探究:
某校研究性学习小组进行了一个有趣的实验探究: