题目内容
1.回收利用是保护金属资源的一条有效途径.某工业废料中含氧化铜和氧化铁,经过一系列处理后可得到铜和硫酸亚铁溶液,主要流程如下.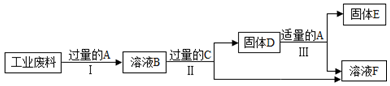
【资料查询】Fe+Fe2(SO4)3═3FeSO4
(1)过程Ⅰ中氧化铁溶解的化学方程式是Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(2)写出溶液B中溶质的化学式:Fe2(SO4)3、CuSO4、H2SO4.
(3)C的化学式为Fe,它发生的反应中属于置换反应的有2个,写出其中一个反应的化学方程式CuSO4+Fe═FeSO4+Cu.
(4)过程Ⅱ充分反应后,还应该有的实验操作是过滤,该操作中所用玻璃仪器有玻璃棒、漏斗和烧杯.
(5)在C~F中,同时含有铁、铜两种元素的是D(填字母代号).
分析 (1)过程Ⅰ中,氧化铁和稀硫酸反应生成硫酸铁和水,氧化铜和稀硫酸反应生成硫酸铁和水;
(2)溶液B中溶质的溶质有反应生成的硫酸铁、硫酸铁和过量的硫酸;
(3)C应该是铁,铁能够硫酸铁反应生成硫酸亚铁,能和硫酸铜反应生成硫酸亚铁和铜,能和稀硫酸反应生成硫酸亚铁和氢气;
(4)过程Ⅱ充分反应后,还应该进行过滤,把液体和固体分离,过滤所用玻璃仪器有玻璃棒、漏斗和烧杯;
(5)根据反应过程可以判断同时含有铁、铜两种元素的物质.
解答 解:(1)过程Ⅰ中,氧化铁和稀硫酸反应生成硫酸铁和水,反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
故填:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(2)溶液B中溶质的溶质有反应生成的硫酸铁、硫酸铁和过量的硫酸.
故填:Fe2(SO4)3、CuSO4、H2SO4.
(3)C是铁,铁的化学式为Fe,铁能够硫酸铁反应生成硫酸亚铁,属于化合反应,能和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:CuSO4+Fe═FeSO4+Cu,属于置换反应,能和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑,属于置换反应.
Fe;2;CuSO4+Fe═FeSO4+Cu.
(4)过程Ⅱ充分反应后,还应该有的实验操作是过滤,该操作中所用玻璃仪器有玻璃棒、漏斗和烧杯.
故填:过滤;玻璃棒、漏斗和烧杯.
(5)在C~F中,同时含有铁、铜两种元素的是D中的反应生成的铜和过量的铁.
故选:D.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
11.对下列物质分类正确的是( )
| A. | 冰和玻璃都是晶体 | B. | 铅笔蕊和陶瓷都属于绝缘体 | ||
| C. | 汞和金刚石都属于金属单质 | D. | 塑料、合成橡胶都属于合成材料 |
12.一种原子的核内有6个质子和6个中子,另一种原子的核内有6个质子和8个中子,则下列说法不正确的是( )
| A. | 它们具有相同的核电荷数 | B. | 它们的质量相同 | ||
| C. | 它们属于同一种元素 | D. | 它们具有相同的核外电子数 |
9.下列物质的用途中,利用其物理性质的是( )
| A. | 液氮用作冷冻剂 | B. | 氧气用作火箭的助燃剂 | ||
| C. | 一氧化碳用作燃料 | D. | 二氧化碳用作光合作用原料 |
16.类推是一种重要的学习方法,下列类推结论正确的是( )
| A. | 乙酸铅能使蛋白质失去生理活性,硫酸铵也能使蛋白质失去生理活性 | |
| B. | NaCl溶于水溶液温度无明显变化,则NH4NO3溶于水溶液温度也无明显变化 | |
| C. | 点燃H2与O2混合气体可能爆炸,则点燃CO与O2的混合气体也可能爆炸 | |
| D. | CuO不能与水反应,则CaO也不能与水反应 |
6.有一瓶未密封保存的氢氧化钠固体,现对其成分进行探究.
(1)猜想:现在这瓶固体的成分可能是氢氧化钠、碳酸钠、氢氧化钠和碳酸钠.
(2)检验氢氧化钠变质的物质是稀盐酸或氯化钙溶液.(填两种不同类别的物质名称)
(3)进一步探究氢氧化钠固体变质的情况.
(1)猜想:现在这瓶固体的成分可能是氢氧化钠、碳酸钠、氢氧化钠和碳酸钠.
(2)检验氢氧化钠变质的物质是稀盐酸或氯化钙溶液.(填两种不同类别的物质名称)
(3)进一步探究氢氧化钠固体变质的情况.
| 实验过程 | 实验现象 | 实验结论 |
| 取少量样品于试管中,加水溶解,向其中加入足量氯化钙溶液 | 产生白色沉淀 | 这瓶固体全部变质 |
| 充分反应后,静置,向上层清液中滴加酚酞试液 | 酚酞试液不变色 |
13.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 酸能使紫色石蕊试液变红,通入CO2后的紫色石蕊试液变红,所以CO2是酸 | |
| B. | 常温下,溶质质量分数24%的硝酸钾溶液是饱和溶液,所以小于24%的硝酸钾溶液一定是不饱和溶液 | |
| C. | 催化剂能改变化学反应速率,某反应的速率发生改变,一定使用了催化剂 | |
| D. | 碱性溶液的 pH大于7,纯碱溶液显碱性,所以纯碱溶液的pH大于7 |
10.石墨烯是由碳原子构成的纳米材料,有良好的强度、柔韧、导电、导热和光学特性.下列关于石墨烯的说法错误的是( )
| A. | 石墨烯可作电极材料 | B. | 石墨烯是一种金属 | ||
| C. | 石墨烯可用于制作包装袋 | D. | 石墨烯完全燃烧生成二氧化碳 |
11.在拓展性课程活动中,小明利用以下常见物品验证酸的一些性质:
白醋(含3%的醋酸)、食品干燥剂(主要成分是CaO)、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠).
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色.
【实验过程】
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊.则鸡蛋壳中一定含有C${{O}_{3}}^{2-}$.(用离子符号表示)
(2)小明知道酸能够与铁发生反应产生氢气,但当他将足量的白醋加入放有铁钉的容器中,没有看到明显的气泡产生.小明很疑惑,于是提出猜想:气泡不明显可能与酸的浓度有关.要验证与酸的浓度有关,应选择下例试剂中的B.(选填编号)
A.3%的盐酸 B.5%的醋酸 C.5%的盐酸
(3)小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计.
【评价反思】科掌来源于生活,生活中的许多事物能更好地帮助我们学习和理解科学.
白醋(含3%的醋酸)、食品干燥剂(主要成分是CaO)、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠).
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色.
【实验过程】
(1)在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊.则鸡蛋壳中一定含有C${{O}_{3}}^{2-}$.(用离子符号表示)
(2)小明知道酸能够与铁发生反应产生氢气,但当他将足量的白醋加入放有铁钉的容器中,没有看到明显的气泡产生.小明很疑惑,于是提出猜想:气泡不明显可能与酸的浓度有关.要验证与酸的浓度有关,应选择下例试剂中的B.(选填编号)
A.3%的盐酸 B.5%的醋酸 C.5%的盐酸
(3)小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计.
| 步骤 | 操作 | 现象 |
| 1 | 将食品干燥剂加入适量清水中,搅拌后静置 | 放出大量的热 |
| 2 | 取步骤1中的上层清液,先加入牵牛花汁液,滴加白醋 | 溶液由无色变为蓝色,再变为紫色,最后变为红色 |