题目内容
12.化学是在原子、分子、离子水平上研究物质及其变化的科学.一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图.
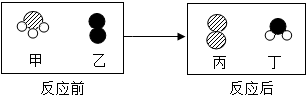
①该反应的前后总共有3种原子;
②该反应是(填“是”或“不是”)置换反应;
③反应前后元素的化合价有(填“有”或“无”)变化;
④在该反应中甲和丁两种分子的个数比为2:3.
分析 观察反应前后微观示意图,根据微粒的构成分析原子的种类、物质的类别、化合价的变化等,根据微粒的变化分析甲、丁两种分子的个数比等.
解答 解:由反应前后微观示意图和质量守恒定律可知,各物质反应的微粒个数关系是:
(1)由微粒的构成可知,反应前后共有3种原子;
(2)由微粒的构成可知,该反应有一种单质与一种化合物反应生成一种单质与一种化合物,是置换反应;
(3)该反应有单质参加和生成,反应前后一定有元素化合价的变化;
(4)由上图可知,该化学反应中,甲、丁两种分子的个数比是2:3;
答案:(1)3;(2)是;(3)有;(4)2:3;
点评 本题是有关微观示意图的考查,学会利用微观的观点及微观示意图的意义对反应基本类型判断及化学变化的微观信息的获取等是解题的关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.两种不含结晶水的晶体A、B的溶解度曲线如图所示.下列分析正确的是( )


| A. | t1℃时,A、B两种物质的饱和溶液中溶质的质量相等 | |
| B. | t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3 | |
| C. | 将t1℃时,A、B两种物质的饱和溶液升温至t2℃,所得溶液的溶质质量分数的大小关系是A>B | |
| D. | 将B的不饱和溶液变为饱和溶液,可采用升温的方法 |
3.实验室常用的制取气体的装置如图:
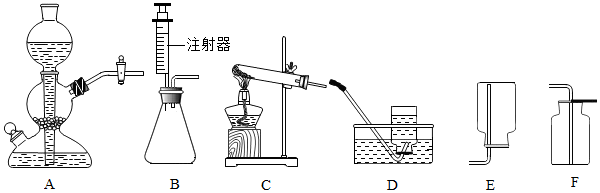
(1)用高锰酸钾制取氧气时,发生反应的方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)收集氧气时,选用装置F的依据是氧气的密度比空气大、不与空气中成分反应,选用装置D收集满的现象是集气瓶口有大气泡冒出;
(3)实验室常用氯化铵固体和碱石灰固体共热来制取氨气,常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水,其水溶液呈碱性,制取并收集氨气,应从如图中选择的发生装置是C,收集装置是E;
(4)在实验室制取二氧化碳的研究中.进行了如下实验:
①上述实验中反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙(填试验编号)对照.
③除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积).
④表中的两个实验.尽管在原料状态、发生装置等方面存在差异,却都能控制气体比较平稳地 产生,请从原枓、操作等方面思考,阐述下表实验中气体比较平稳产生的最主要的一个原因.

(1)用高锰酸钾制取氧气时,发生反应的方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)收集氧气时,选用装置F的依据是氧气的密度比空气大、不与空气中成分反应,选用装置D收集满的现象是集气瓶口有大气泡冒出;
(3)实验室常用氯化铵固体和碱石灰固体共热来制取氨气,常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水,其水溶液呈碱性,制取并收集氨气,应从如图中选择的发生装置是C,收集装置是E;
(4)在实验室制取二氧化碳的研究中.进行了如下实验:
| 药品、实验编号 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
②若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙(填试验编号)对照.
③除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积).
④表中的两个实验.尽管在原料状态、发生装置等方面存在差异,却都能控制气体比较平稳地 产生,请从原枓、操作等方面思考,阐述下表实验中气体比较平稳产生的最主要的一个原因.
| 目的 | 原料 | 发生装置 | 气体比较平稳产生的最主要一个原因 |
| 制取二氧化碳 | 块状大理石 稀盐酸 | A | |
| 制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | B |
20.下列排列顺序正确的是( )
| A. | 常见物质的pH$→_{由小到大}^{肥皂水食盐水醋酸}$ | |
| B. | 氯元素的化合价$→_{由低到高}^{HClCa(ClO)_{2}NaClO_{2}}$ | |
| C. | 人体中元素含量$→_{由低到高}^{CaZnFe}$ | |
| D. | 硫元素的质量分数$→_{由低到高}^{Na_{2}SO_{3}Na_{2}SO_{4}Na_{2}S}$ |
7.下列说法正确的是( )
| A. | 含有碳元素的物质都是有机物 | |
| B. | 合金的硬度一般比各成分金属小 | |
| C. | 用灯帽盖灭酒精灯,是为了降低可燃物的温度 | |
| D. | 室内开花,墙外可以嗅到花香,说明分子在不断的运动 |
17.根据如图有关信息判断,下列说法错误的是( )


| A. | 镁元素的相对原子质量为12 | |
| B. | 在化学反应中,镁原子容易失去2个电子 | |
| C. | 在元素周期表中,镁元素和钙元素属于同一个族 | |
| D. | 钙离子核内有20个质子 |
9.苯甲酸是一种食品防腐剂,它是一种片状晶体,在水中的溶解度如表:
某同学为了提纯某一苯甲酸样品(其中含泥沙等难溶于水的杂质),进行了如下实验:
(1)取样品约1g放入烧杯中,加入50mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是常温下苯甲酸溶解度很小.
(2)将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤.趁热过滤的目的是减小过滤时苯甲酸的损失.
(3)将所得滤液缓慢降温至室温,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体.
| 温度℃ | 25 | 50 | 95 |
| 溶解度g | 0.17 | 0.95 | 6.8 |
(1)取样品约1g放入烧杯中,加入50mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是常温下苯甲酸溶解度很小.
(2)将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤.趁热过滤的目的是减小过滤时苯甲酸的损失.
(3)将所得滤液缓慢降温至室温,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体.
