题目内容
8.在一定条件下,锌与稀硝酸可发生反应:4Zn+10HNO3=4Zn(NO3)2+□X+N2O↑,其中X为一种常见物质.关于物质X,下列说法正确的是( )| A. | X的化学式为H2O2 | B. | X前面的计量系数为5 | ||
| C. | X中两种元素的质量比为1:16 | D. | X中元素化合价为零 |
分析 根据反应的化学方程式4Zn+10HNO3=4Zn(NO3)2+□X+N2O↑,利用反应前后原子种类、数目不变,推断反应生成物X的分子构成、确定该物质X的化学式.
解答 解:反应的化学方程式4Zn+10HNO3=4Zn(NO3)2+□X+N2O↑,反应物中含Zn、H、N、O四种元素的原子个数分别为4、10、10、30,反应后生成物中含Zn、H、N、O四种元素的原子个数分别为4、0、10、25,根据反应前后原子种类、数目不变,可判断X中含10个H原子和5个O原子,则X的化学式为H2O,故A错,前边的计量数是5,故B正确;H2O中氢元素和氧元素的质量比是2:16=1:8,故C错,水中氢元素化合价是+1价,氧元素化合价是-2价,故D错.
故选B.
点评 根据反应的化学方程式,利用反应前后原子种类、数目不变,可推断反应中某物质的分子构成、确定该物质的化学式

练习册系列答案
相关题目
18.已知CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2可溶于水.下列图象不能正确反映其对应变化关系的是
( )
( )
| A. | 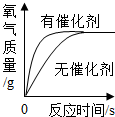 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 | |
| B. | 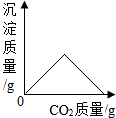 表示澄清石灰水中持续通入CO2 表示澄清石灰水中持续通入CO2 | |
| C. | 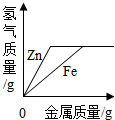 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉 | |
| D. | 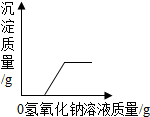 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 |
16. 地壳中含有丰富的氧、硅、铝、铁等元素.结合如图分析,关于这四种元素的说法错误的是( )
地壳中含有丰富的氧、硅、铝、铁等元素.结合如图分析,关于这四种元素的说法错误的是( )
 地壳中含有丰富的氧、硅、铝、铁等元素.结合如图分析,关于这四种元素的说法错误的是( )
地壳中含有丰富的氧、硅、铝、铁等元素.结合如图分析,关于这四种元素的说法错误的是( )| A. | 氧原子的核电荷数为8 | |
| B. | 硅元素属于非金属元素 | |
| C. | 铝与氧元素形成化合物的化学式为A1203 | |
| D. | 铁的相对原子质量为55.85g |
3.目前,环境保护部正在着力推进防治PM2.5为重点的大气污染防治工作.
(1)PM2.5监测数据中的“2.5”是指C.
A、空气污染指数B、噪音的大小C、空气中颗粒的直径D、有害气体的浓度
(2)防PM2.5的专用口罩里含有活性炭,这是利用了活性炭吸附性功能.
(3)某地一年四季空气质量监测的平均数据如下表,对该地空气质量影响最大的指标是可吸入颗粒物.
(4)空气质量级别数值越大,空气的质量状况越差(填“好”或“差”或“无影响,).
(5)使用二甲醚(化学式C2H60)为燃料的城市客车,能减少汽车尾气中PM2.5的排放.二甲醚燃烧的化学方程式为C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.二甲醚燃烧驱动汽车的过程是化学能能转化为热能继而转化为机械能的过程.
(6)某稀薄燃烧汽车发动机中的汽油喷成雾状,汽油与空气的质量比高达1:25以上,而普通汽车发动机中汽油与空气的质量比为1:15,试从微观的角度加以解释这样做的原因增大了可燃物分子与氧气分子的接触面积,使汽油燃烧充分.
(1)PM2.5监测数据中的“2.5”是指C.
A、空气污染指数B、噪音的大小C、空气中颗粒的直径D、有害气体的浓度
(2)防PM2.5的专用口罩里含有活性炭,这是利用了活性炭吸附性功能.
(3)某地一年四季空气质量监测的平均数据如下表,对该地空气质量影响最大的指标是可吸入颗粒物.
| 可吸入颗粒物 | 氮氧化合物 | 二氧化硫 | 空气质量级别 | |
| 春季 | 88 | 40 | 44 | Ⅱ |
| 夏季 | 67 | .33 | 36 | Ⅱ |
| 秋季 | 90 | 46 | 54 | Ⅱ |
| 冬季 | 98 | 69 | 60 | Ⅱ |
(5)使用二甲醚(化学式C2H60)为燃料的城市客车,能减少汽车尾气中PM2.5的排放.二甲醚燃烧的化学方程式为C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.二甲醚燃烧驱动汽车的过程是化学能能转化为热能继而转化为机械能的过程.
(6)某稀薄燃烧汽车发动机中的汽油喷成雾状,汽油与空气的质量比高达1:25以上,而普通汽车发动机中汽油与空气的质量比为1:15,试从微观的角度加以解释这样做的原因增大了可燃物分子与氧气分子的接触面积,使汽油燃烧充分.
20.下列化学方程式符合题意,且书写正确的是( )
| A. | 铁与稀盐酸反应:2Fe+6HCl═2FeCl3+3H2↑ | |
| B. | 铁丝在氧气中燃烧:3Fe+2O2═Fe3O4 | |
| C. | 利用一氧化碳的还原性冶炼金属:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$ Cu+CO2 | |
| D. | 食盐溶于硝酸钾溶液:NaCl+KNO3═NaNO3+KCl |