题目内容
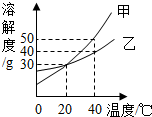
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )

| A、乙中混有少量甲时,可以用冷却热饱和溶液的方法提纯乙 |
| B、40℃时,分别在100g水中加入50g甲、乙,所得溶液溶质质量分数相等 |
| C、20℃时,甲、乙两种物质的饱和溶液中溶质的质量相等 |
| D、40℃时,甲溶液中溶质的质量分数不一定大于乙溶液中溶质质量分数 |
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、根据甲、乙的溶解度随温度变化情况分析提纯乙的方法
B、40℃时甲物质的溶解度是50g,乙物质的溶解度是40g,在100g水中,加入50g甲全部溶解,加入50g乙不能全部溶解,根据饱和时质量分数的计算式
×100%=
×100%,
C、20℃由于甲乙两饱和溶液的质量不一定相等,故无法比较所含溶质的质量,一定温度下的饱和溶液中,溶解度相等则溶质的质量分数也相等;
D、40℃时,虽然甲的溶解度大于乙的溶解度,但不知溶液是否饱和,甲溶液中溶质的质量分数不一定大于乙溶液中溶质质量分数;
B、40℃时甲物质的溶解度是50g,乙物质的溶解度是40g,在100g水中,加入50g甲全部溶解,加入50g乙不能全部溶解,根据饱和时质量分数的计算式
| 溶解度 |
| 溶解度+100g |
| 1 | ||
1+
|
C、20℃由于甲乙两饱和溶液的质量不一定相等,故无法比较所含溶质的质量,一定温度下的饱和溶液中,溶解度相等则溶质的质量分数也相等;
D、40℃时,虽然甲的溶解度大于乙的溶解度,但不知溶液是否饱和,甲溶液中溶质的质量分数不一定大于乙溶液中溶质质量分数;
解答:解:
A、甲的溶解度随温度的升高,B的溶解度随温度的升高变化较小,乙中混有少量甲时,可以用蒸发结晶的方法提纯乙,故说法错误;
B、40℃时甲物质的溶解度是50g,乙物质的溶解度是40g,在100g水中,加入50g甲全部溶解,加入50g乙不能全部溶解,根据饱和时质量分数的计算式
×100%=
×100%,即溶解度越大质量分数也就越大,所以此时溶液的质量分数关系是A>B,故说法错误;
C、20℃由于甲乙两饱和溶液的质量不一定相等,故无法比较所含溶质的质量,故说法错误;
D、40℃时,虽然甲的溶解度大于乙的溶解度,但不知溶液是否饱和,甲溶液中溶质的质量分数不一定大于乙溶液中溶质质量分数,故说法正确;
答案:D
A、甲的溶解度随温度的升高,B的溶解度随温度的升高变化较小,乙中混有少量甲时,可以用蒸发结晶的方法提纯乙,故说法错误;
B、40℃时甲物质的溶解度是50g,乙物质的溶解度是40g,在100g水中,加入50g甲全部溶解,加入50g乙不能全部溶解,根据饱和时质量分数的计算式
| 溶解度 |
| 溶解度+100g |
| 1 | ||
1+
|
C、20℃由于甲乙两饱和溶液的质量不一定相等,故无法比较所含溶质的质量,故说法错误;
D、40℃时,虽然甲的溶解度大于乙的溶解度,但不知溶液是否饱和,甲溶液中溶质的质量分数不一定大于乙溶液中溶质质量分数,故说法正确;
答案:D
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以培养学生应用知识解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 在天平左右托盘上,各放一质量相等的烧杯,其盛有质量相等的稀硫酸,天平平衡,如果将下列四组物质分虽加入左右托盘内,充分反应后,天平仍保持平衡的是( )
在天平左右托盘上,各放一质量相等的烧杯,其盛有质量相等的稀硫酸,天平平衡,如果将下列四组物质分虽加入左右托盘内,充分反应后,天平仍保持平衡的是( )| A、等质量的锌和铜 |
| B、等质量的铁和铜 |
| C、等质量的锌和铁(反应后烧杯中两种金属均有剩余) |
| D、等质量的锌和铁(反应后烧杯内酸都有剩余) |
下列各组溶液,不加其他试剂就能鉴别的是( )
| A、AgNO3、NaCl、CaCl2、HNO3 |
| B、NaOH、NaCl、K2NO3、稀HCl |
| C、BaCl2、Na2SO4、K2CO3、HNO3 |
| D、CuSO4、NaCl、KNO3、BaCl2 |
下列各组气体中既能用浓硫酸干燥,又能用苛性钠干燥的是( )
| A、CO2、HCl |
| B、H2、O2 |
| C、SO2、CO |
| D、SO2、CO2 |
将CaO和Na2O两种碱性氧化物的混合物溶解于水,加入足量的K2CO3溶液充分应后过滤,得干燥的白沉淀,测得白色沉淀的质量与原混合物的质量相等.则原混合物中Na2O的质量分数为( )
| A、60% | B、56% |
| C、44% | D、40% |
用墨书写的字画,虽年长日久但仍不褪色,这是因为墨的主要成分-碳( )
| A、不跟其他任何物质反应 |
| B、常温下,化学性质稳定 |
| C、易与纸张反应生成化学性质稳定的物质 |
| D、任何条件下化学性质均稳定 |
下列实验结论正确的是( )
| A、向某无色溶液中滴加酚酞试液无现象,则溶液一定呈中性 |
| B、向某固体中滴加稀盐酸,有气泡产生,该固体一定是碳酸盐 |
| C、能和碱反应生成盐和水的物质一定是酸性氧化物 |
| D、盐的组成可能不含金属元素 |
如图形象地表示基本化学反应前后反应物与生成物分子及其数目的变化,其中 分别表示A、B、C三种不同的分子.则参加反应的A、B与生成的C的分子个数之比为( )
分别表示A、B、C三种不同的分子.则参加反应的A、B与生成的C的分子个数之比为( )
 分别表示A、B、C三种不同的分子.则参加反应的A、B与生成的C的分子个数之比为( )
分别表示A、B、C三种不同的分子.则参加反应的A、B与生成的C的分子个数之比为( )
| A、4:1:3 |
| B、1:3:2 |
| C、4:1:2 |
| D、3:1:3 |
 人类的生存离不开氧气,某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
人类的生存离不开氧气,某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.