题目内容
 在天平左右托盘上,各放一质量相等的烧杯,其盛有质量相等的稀硫酸,天平平衡,如果将下列四组物质分虽加入左右托盘内,充分反应后,天平仍保持平衡的是( )
在天平左右托盘上,各放一质量相等的烧杯,其盛有质量相等的稀硫酸,天平平衡,如果将下列四组物质分虽加入左右托盘内,充分反应后,天平仍保持平衡的是( )| A、等质量的锌和铜 |
| B、等质量的铁和铜 |
| C、等质量的锌和铁(反应后烧杯中两种金属均有剩余) |
| D、等质量的锌和铁(反应后烧杯内酸都有剩余) |
考点:金属的化学性质
专题:金属与金属材料
分析:金属和酸反应会放出氢气,只有两个烧杯中加入的金属质量相等,放出的氢气质量也相等,天平才能仍然保持平衡
解答:解:
A、加入等质量的锌和铜,因为锌和稀硫酸反应放出氢气,而铜和稀硫酸不反应,所以天平不平衡,加铜的一侧天平会下降.故A错误;
B、加入等质量的铁和铜,因为铁和稀硫酸反应放出氢气,而铜和稀硫酸不反应,所以天平也不平衡,加铜的一侧天平会下降.故B错误;
C、加入等质量的锌和铁,因为反应后烧杯中两种金属均有剩余,说明两烧杯中的酸都完全反应,而两烧杯中的稀硫酸是等量的,所以产生的氢气也是相等的,即两烧杯中的质量增加量相等,所以天平仍然平衡.故C正确;
D、加入等质量的锌和铁,因为反应后烧杯内酸都有剩余,所以金属都完全反应,而等质量的锌与酸反应放出的氢气比等质量的铁与酸反应放出的氢气少,所以天平不平衡,加锌的一侧天平会下降.故D错误.
故选:C.
A、加入等质量的锌和铜,因为锌和稀硫酸反应放出氢气,而铜和稀硫酸不反应,所以天平不平衡,加铜的一侧天平会下降.故A错误;
B、加入等质量的铁和铜,因为铁和稀硫酸反应放出氢气,而铜和稀硫酸不反应,所以天平也不平衡,加铜的一侧天平会下降.故B错误;
C、加入等质量的锌和铁,因为反应后烧杯中两种金属均有剩余,说明两烧杯中的酸都完全反应,而两烧杯中的稀硫酸是等量的,所以产生的氢气也是相等的,即两烧杯中的质量增加量相等,所以天平仍然平衡.故C正确;
D、加入等质量的锌和铁,因为反应后烧杯内酸都有剩余,所以金属都完全反应,而等质量的锌与酸反应放出的氢气比等质量的铁与酸反应放出的氢气少,所以天平不平衡,加锌的一侧天平会下降.故D错误.
故选:C.
点评:此题考查的是活泼金属与酸反应的性质,重点要把金属活动顺序表背过,分清哪种金属和酸反应哪种金属和酸不反应,另外要能根据酸和金属反应的化学方程式来判断等质量的金属哪个放出的氢气多.难度适中,属于常见题型.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
以下说法正确的是( )
| A、澄清透明的液体一定是溶液 |
| B、溶液中的溶质不可能是液体或气体 |
| C、洗涤剂除油污的过程利用的乳化作用 |
| D、将氯化钠溶液长期露置于空气中,溶液中的氯化钠也不会析出 |
密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:下列说法正确的是( )
| 物质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 31.6 | 0.4 |
| 反应后质量/g | 待测 | 20.6 | 0 | 0.4 |
| A、物质C一定是化合物,物质D不可能是单质 |
| B、反应后密闭容器中A的质量为19.7g |
| C、反应过程中,物质B与物质D变化的质量比为87:36 |
| D、若物质A与物质C的相对分子质量之比为197:158,则反应中A与C的化学计量数之比为1:2 |
“达菲”是治疗人类感染禽流感的一种药物,而合成“达菲”的主要原料莽草酸(化学式C7H10O5)存在于我国盛产的八角茴香中,下列说法正确的是( )
| A、每个莽草酸分子中含有21个原子 |
| B、莽草酸的相对分子质量为87 |
| C、莽草酸中碳、氢、氧三种元素的质量比为42:5:40 |
| D、莽草酸中碳元素的质量分数约为21% |
下列物质在氧气中燃烧时,能产生无色气体的是( )
| A、红磷 | B、木条 | C、铁丝 | D、镁带 |
若正确量取48mL的液体,最适合的仪器是( )
| A、100mL的量筒 |
| B、50mL的量筒 |
| C、烧杯 |
| D、胶头滴管 |
为了加强人民体质,市政府决定进行“食盐加碘”工程.这里的碘是指( )
| A、分子 | B、元素 | C、原子 | D、化合物 |
在实验室的下列做法中正确的是( )
| A、为了节约药品,用剩的药品应放回原试剂瓶 | ||
| B、为了获得感性认识,可触摸药品或尝药品的味道 | ||
| C、为了能看到标签,倾倒试液时,标签不能向着手心 | ||
D、为了安全,向酒精灯内添加酒精不能超过其容积的
|
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
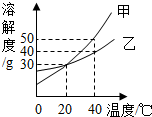

| A、乙中混有少量甲时,可以用冷却热饱和溶液的方法提纯乙 |
| B、40℃时,分别在100g水中加入50g甲、乙,所得溶液溶质质量分数相等 |
| C、20℃时,甲、乙两种物质的饱和溶液中溶质的质量相等 |
| D、40℃时,甲溶液中溶质的质量分数不一定大于乙溶液中溶质质量分数 |